Розділ: Основні класи неорганічних сполук
Тема: Амфотерні сполуки
Кількість завдань: 50
ТЕМА: Реакції металів із кислотами й солей із лугами. Осадження гідроксидів.
Завдання скеровано на перевірку вміння прогнозувати продукти реакцій металів із кислотами, солей із лугами у водних розчинах.
1.
Залишок на фільтрі – магній гідроксид – гідроксид металічного елемента (А).
2.
Залишок на фільтрі – мідь – метал (Б).
3.
Залишок на фільтрі – мідь і магній гідроксид – метал і гідроксид металічного елемента (В).
Відповідь: 1А; 2Б; 3В.
ТЕМА: Хімічні властивості основних класів неорганічних сполук.
Завдання скеровано на перевірку вміння за хімічною формулою визначати тип кристалічних ґраток речовини й прогнозувати її хімічні властивості.
| Варіант відповіді | 1 | 2 | 3 |
| А | |||
| Б | |||
| B | |||
| Г |
Натрій гідроксид
Відповідь: Г.
ТЕМА: Загальна хімія. Основні класи неорганічних сполук.
Завдання скеровано на перевірку вміння прогнозувати продукти реакцій між неорганічними речовинами.
Речовина 1 не взаємодіє з водою і хлоридною кислотою, але реагує з натрій гідроксидом. Це кислотний силіцій(IV) оксид:
Речовина 2 реагує з водою і натрій гідроксидом, але не взаємодіє з хлоридною кислотою. Це кислотний фосфор(V) оксид:
Речовина 3 не взаємодіє з водою, , але реагує з натрій гідроксидом і хлоридною кислотою. Це амфотерний алюміній оксид:
Відповідь: 1Г; 2Д; 3В.
ТЕМА: Неорганічна хімія. Амфотерність. Цинк оксид і цинк гідроксид.
Завдання скеровано на перевірку розуміння суті амфотерності.
Амфотерність – здатність речовин реагувати і з кислотами, і з лугами.
Цинк оксид є амфотерним гідроксидом, бо реагує з кислотами як основний оксид, а з лугами – як кислотний.
Відповідь: Б.
ТЕМА: Неорганічна хімія. Основні класи неорганічних сполук. Амфотерні сполуки.
Завдання скеровано на перевірку розуміння суті амфотерності.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості. З кислотами алюміній гідроксид
Відповідь: Г.
ТЕМА: Неорганічна хімія. Неорганічні речовини і їхні властивості. Амфотерні оксиди й гідроксиди.
Завдання скеровано на перевірку розуміння суті амфотерності й уміння розпізнавати амфотерні оксиди й гідроксиди.
Амфотерність – здатність сполуки реагувати з лугами як кислота, а з кислотами – як основа.
Умову завдання задовольняє варіант відповіді B. У цьому рядку наведено формули амфотерних оксидів Цинку й Алюмінію і амфотерного алюміній гідроксиду.
Відповідь: B.
ТЕМА: Неорганічна хімія. Основні класи неорганічних сполук. Амфотерні сполуки.
Завдання скеровано на перевірку розуміння суті амфотерності, уміння розпізнавати формули амфотерних оксидів і гідроксидів.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості.
З кислотами алюміній оксид і цинк гідроксид реагують як основні, із лугами – як кислотні, тобто виявляють амфотерні властивості:
Відповідь: A.
ТЕМА: Неорганічні речовини і їхні властивості. Амфотерність. Алюміній гідроксид.
Завдання скеровано на перевірку розуміння суті амфотерності.
Амфотерність – здатність деяких хімічних сполук залежно від умов виявляти або основні, або кислотні властивості.
Алюміній гідроксид амфотерний, тобто здатний залежно від умов виявляти або осно́вні, або кислотні властивості. З кислотами алюміній гідроксид
Тобто лише в досліді Г йдеться про амфотерні властивості алюміній гідроксиду:
Відповідь: Г.
ТЕМА: Неорганічні речовини і їхні властивості. Амфотерність. Алюміній гідроксид.
Завдання скеровано на перевірку розуміння суті амфотерності.
Осади гідроксидів Магнію, Калію, Феруму(ІІ) розчиняться в кислоті й не розчиняться в надлишку розчину лугу.
Алюміній гідроксид амфотерний, тобто здатний залежно від умов виявляти або осно́вні, або кислотні властивості. З кислотами алюміній гідроксид
Тобто речовина
Відповідь: B.
ТЕМА: Явище амфотерності.
Завдання скеровано на перевірку розуміння суті амфотерності, уміння аналізувати й прогнозувати результати дослідження, робити висновки.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або основні, або кислотні властивості. Прикладами амфотерних оксидів є оксиди Цинку й Алюмінію.
Відповідь: Б.
ТЕМА: Неорганічна хімія. Неорганічні речовини і їхні властивості. Алюміній і залізо.
Завдання скеровано на перевірку вміння прогнозувати можливість перебігу хімічних реакцій між неорганічними речовинами.
Твердження Г є неправильним, бо алюміній оксид – малоактивна речовина. Алюміній гідроксид добувають реакцією обміну між солями Алюмінію і лугами в розчині.
Інші наведені в умові завдання твердження правильні:
A |
|
Б |
|
B |
Відповідь: Г.
ТЕМА: Неорганічна хімія. Неорганічні речовини і їхні властивості. Амфотерні сполуки.
Завдання скеровано на перевірку розуміння суті амфотерності.
Амфотерність – здатнiсть сполуки виявляти кислотнi або основнi властивостi залежно вiд природи реагенту.
Умову завдання задовольняє варіант відповіді Б, у якому наведено схеми реакцій цинк оксиду як із кислотою, так і з лугом. Це доводить його амфотерність.
Відповідь: Б.
ТЕМА: Основні класи неорганічних сполук. Амфотерні сполуки.
Завдання скеровано на перевірку знання про амфотерні сполуки.
Для виконання завдання необхідно знати, які металічні елементи можуть утворювати амфотерні сполуки.
Із запропонованих варіантів відповіді лише алюміній гідроксид і цинк гідроксид виявляють амфотерні властивості.
Відповідь: Б.
ТЕМА: Електроліти. Електролітична дисоціація.
Завдання скеровано на перевірку вміння прогнозувати продукти електролітичної дисоціації.
У водному розчині з утворенням катіонів Гідрогену дисоціюють нітратна кислота (1), гідроген хлорид (4) і сульфітна кислота (5).
Відповідь: Г.
ТЕМА: Неорганічні речовини і їхні властивості. Амфотерність.
Завдання скеровано на перевірку розуміння суті амфотерності, уміння аналізувати й прогнозувати результати дослідження, робити висновки.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості. З кислотами цинк оксид реагує як осно́вний, із лугами – як кислотний.
Відповідь: B.
ТЕМА: Основні класи неорганічних сполук. Солі. Амфотерні сполуки.
Завдання перевіряє знання хімічних властивостей амфотерних сполук, а саме амфотерних гідроксидів, та їхню взаємодію з кислотами і лугами.
Для розв’язання завдання необхідно знати і розуміти, що цинк нітрат реагує з лугом з утворенням осаду – амфотерного цинк гідроксиду, який розчиняється як у надлишку лугу, так і в надлишку кислоти.
Відповідь: B
ТЕМА: Неорганічна хімія. Основні класи неорганічних сполук. Амфотерні сполуки.
Завдання перевіряє знання явища амфотерності.
Для виконання завдання необхідно знати, сполуки яких елементів можуть виявляти амфотерні властивості. У завданні наведено назви чотирьох оксидів. Оксиди Натрію, Калію й Барію виявляють основні властивості, тому що ці елементи є типовими металами, а оксид Цинку виявляє амфотерні властивості.
Відповідь: A.
ТЕМА: Неорганічні речовини і їхні властивості. Алюміній.
Завдання скеровано на перевірку знання властивостей будови атома Алюмінію, властивостей алюмінію і сполук Алюмінію, способів їхнього добування.
A |
У хімічних реакціях атоми Алюмінію віддають електрони й окиснюються |
Б |
У йона Алюмінію така сама (10 електронів) електронна конфігурація, як в атома Неону |
B |
алюміній гідроксид не добувають реакцією алюміній оксиду з водою. Його добувають реакцією обміну між сіллю алюмінію і лугом у водному розчині |
Г |
оксид і гідроксид Алюмінію амфотерні, тому можуть реагувати як із кислотами, так і з лугами, зокрема з натрій гідроксидом |
Відповідь: Г.
ТЕМА: Неорганічні речовини і їхні властивості. Амфотерність.
Завдання скеровано на перевірку розуміння суті амфотерності, уміння аналізувати й прогнозувати результати дослідження, робити висновки.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості. З кислотами цинк оксид реагує як осно́вний, із лугами – як кислотний. Тобто амфотерні властивості цинк оксиду описані перетвореннями, наведеними в рядку Б.
Відповідь: Б.
ТЕМА: Основні класи неорганічних сполук. Солі. Амфотерні сполуки.
Завдання перевіряє знання хімічних властивостей сполук амфотерних елементів і вміння складати рівняння реакцій взаємодії солей амфотерних елементів з лугами в розчині.
Для виконання завдання необхідно знати, що алюміній хлорид – сіль амфотерного елемента й розуміти, що солі амфотерних елементів реагують з лугом з утворенням осаду, який розчиняється в надлишку лугу.
Відповідь: B.
ТЕМА: Неорганічні речовини і їхні властивості. Амфотерність. Цинк гідроксид.
Завдання скеровано на перевірку розуміння суті амфотерності.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості. З кислотами цинк гідроксид
Відповідь: Г.
ТЕМА: Неорганічні речовини і їхні властивості. Амфотерність. Алюміній гідроксид.
Завдання скеровано на перевірку розуміння суті амфотерності.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості. З кислотами алюміній гідроксид реагує як основа, із лугами – як кислота, тобто виявляє амфотерні властивості.
Тож для доведення його амфотерності потрібно використати сульфатну кислоту й натрій гідроксид:
Відповідь: B.
ТЕМА: Неорганічні речовини і їхні властивості. Амфотерність.
Завдання скеровано на перевірку розуміння суті амфотерності, уміння розпізнавати амфотерні оксиди.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості. З кислотами цинк оксид
Відповідь: A.
ТЕМА: Загальні відомості про металічні елементи й метали. Алюміній, сполуки Алюмінію.
Завдання скеровано на перевірку знання хімічних властивостей алюмінію, сполук Алюмінію.
I Алюміній належить до p-елементів, в його атомі заповнюється електронами p-підрівень:
II Алюміній гідроксид за нагрівання розкладається:
III У йона
IV Для добування водню в лабораторії можна використати алюміній і хлоридну кислоту:
Відповідь: Г.
ТЕМА: Неорганічні речовини і їхні властивості. Амфотерність.
Завдання скеровано на перевірку розуміння суті амфотерності.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості. З кислотами цинк гідроксид
Цинкати – солі слабкої кислоти, тому під дією сильних кислот руйнуються:
Відповідь: Г.
ТЕМА: Неорганічні речовини і їхні властивості. Амфотерність.
Завдання скеровано на перевірку розуміння суті амфотерності.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості. З кислотами алюміній гідроксид
Відповідь: Г.
ТЕМА: Загальна хімія. Основні класи неорганічних сполук.
Завдання скеровано на перевірку вміння класифікувати неорганічні речовини.
1
2
3
4
Відповідь: Б, А, Д, Б.
ТЕМА: Оксиди. Амфотерність.
Завдання скеровано на перевірку розуміння суті амфотерності й уміння розпізнавати амфотерні оксиди.
Класифікацію оксидів за їхнім складом і хімічними властивостями наведено на рисунку 1.
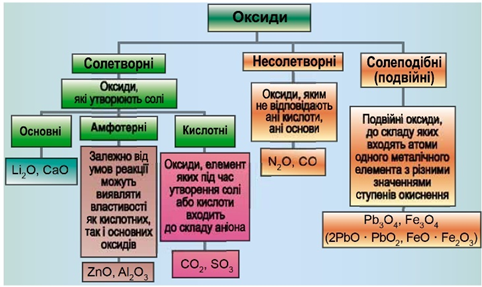
Рис. 1. Класифікація оксидів
Ферум(ІІ) оксид основний, а алюміній оксид амфотерний.
Основні оксиди реагують з кислотами й не реагують із лугами.
Амфотерні оксиди реагують і з кислотами, і з лугами.
Якщо додати до суміші цих двох оксидів розчин лугу й профільтрувати, прореагує і перейде в розчин лише алюміній оксид, а на фільтрі залишиться ферум(ІІ) оксид.
Відповідь: Г.
ТЕМА: Алюміній оксид. Амфотерність.
Завдання скеровано на перевірку розуміння суті амфотерності, знання властивостей алюміній оксиду.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або основні, або кислотні властивості. Наприклад, з кислотами алюміній оксид реагує як основний, з лугами – як кислотний:
Відповідь: Г.
ТЕМА: Неорганічна хімія. Амфотерні оксиди й гідроксиди.
Завдання скеровано на перевірку розуміння суті амфотерності.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або основні, або кислотні властивості. Наприклад, з кислотами гідроксиди Алюмінію та Цинку реагують як основи, з лугами – як кислоти.
На схемі 1 відображено реакцію цинку з хлоридною кислотою. На схемі 2 – добування цинк гідроксиду реакцією обміну між сіллю і лугом у водному розчині.
На схемах 3 й 4 відображено реакції цинк оксиду з кислотою і лугом відповідно, тобто його амфотерні властивості.
Відповідь: Г.
ТЕМА: Неорганічні речовини і їхні властивості. Амфотерність. Алюміній гідроксид.
Завдання скеровано на перевірку розуміння суті амфотерності.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості. З кислотами алюміній гідроксид
Відповідь: Г.
ТЕМА: Неорганічні речовини і їхні властивості. Амфотерність.
Завдання скеровано на перевірку розуміння суті амфотерності й уміння розпізнавати амфотерні оксиди.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості. Оксиди й гідроксиди Магнію виявляють осно́вні властивості й реагують із кислотами. Оксиди Цинку й Алюмінію виявляють амфотерні властивості:
Відповідь: Г.
ТЕМА: Явище амфотерності.
Завдання скеровано на перевірку розуміння суті амфотерності, уміння аналізувати й прогнозувати результати дослідження, робити висновки.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або основні, або кислотні властивості. Наприклад, із кислотами цинк оксид реагує як основний, із лугами – як кислотний:
Відповідь: Г.
ТЕМА: Неорганічні речовини і їхні властивості. Амфотерність.
Завдання скеровано на перевірку розуміння суті амфотерності.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості. Цинк гідроксид реагує як із кислотами, так і з лугами, тобто є амфотерним:
Відповідь: Г.
ТЕМА: Неорганічна хімія. Основні класи неорганічних сполук.
Завдання скеровано на перевірку вміння розпізнавати неорганічні речовини різних класів.
Речовина (1) утворена катіонами Кальцію і карбонат-аніонами – кальцій карбонат, сіль (Г).
Речовина (2) містить атоми Гідрогену й кислотний залишок силікат – силікатна кислота (В).
Речовина (3) утворена катіонами Алюмінію і гідроксид-аніонами – амфотерний алюміній гідроксид (Д).
Речовина (4) – сульфур(IV) оксид, бінарна сполука Сульфуру й Оксигену, у молекулах якої ступінь окиснення атомів Оксигену становить –2 (А).
Відповідь: 1Г, 2В, 3Д, 4А.
ТЕМА: Неорганічні речовини і їхні властивості. Алюміній гідроксид.
Завдання скеровано на перевірку розуміння суті явища амфотерності.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості.
Для доведення амфотерності алюміній гідроксиду потрібно використати луг і кислоту:
Відповідь: A.
ТЕМА: Неорганічні речовини і їхні властивості. Амфотерність.
Завдання скеровано на перевірку розуміння суті амфотерності й уміння розпізнавати амфотерні оксиди.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості. Оксиди й гідроксиди Магнію і Кальцію виявляють осно́вні властивості й реагують із кислотами. Оксид і гідроксид Цинку виявляють амфотерні властивості:
Відповідь: B.
ТЕМА: Неорганічні речовини і їхні властивості. Амфотерність.
Завдання скеровано на перевірку розуміння суті амфотерності й уміння розпізнавати амфотерні оксиди й гідроксиди.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості. Оксиди й гідроксиди Цинку й Алюмінію виявляють амфотерні властивості:
Відповідь: Б.
ТЕМА: Неорганічні речовини і їхні властивості. Амфотерність.
Завдання скеровано на перевірку розуміння суті амфотерності, уміння пояснювати результати дослідів.
Алюміній гідроксид – нерозчинна у воді сполука, тому його можна добути реакцією обміну між розчинною сіллю Алюмінію і лугом у водному розчині:
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості. З кислотами алюміній гідроксид
Тому осад алюміній гідроксиду розчиняється і в кислоті, і в лугу:
Відповідь: B.
ТЕМА: Неорганічні речовини і їхні властивості. Амфотерність.
Завдання скеровано на перевірку розуміння суті амфотерності.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості. Оксиди й гідроксиди Барію, Кальцію, Стронцію виявляють осно́вні властивості й реагують з кислотами. Цинк оксид і цинк гідроксид реагують як з кислотами, так і з лугами, тобто є амфотерними:
Відповідь: Б.
ТЕМА: Загальна хімія. Основні класи неорганічних сполук. Оксиди.
Завдання скеровано на перевірку вміння розпізнавати основні, кислотні, амфотерні оксиди.
Класифікацію оксидів за їхнім складом і хімічними властивостями наведено на рисунку 1.
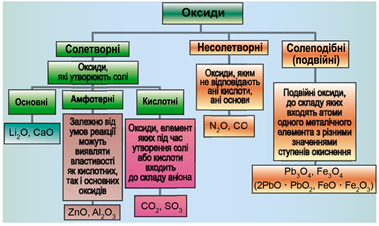
Рис. 1. Класифікація оксидів
До основних оксидів належать:
- оксиди всіх металічних елементів головної підгрупи першої групи;
- оксиди всіх металічних елементів головної підгрупи другої групи, починаючи з магнію
\((\mathrm{Mg\ –\ Ra})\) ; - оксиди металічних елементів у нижчих значеннях валентності, наприклад
\(\mathrm{MnO, FeO}\) .
Кислотними оксидами є більшість оксидів неметалічних елементів (
Амфотерні оксиди під час взаємодії з кислотою або кислотним оксидом виявляють властивості, характерні для основних оксидів. Так само, як основні оксиди, вони взаємодіють з кислотами з утворенням солі і води. У реакціях із лугами або з оксидами лужних і лужноземельних елементів амфотерні оксиди виявляють кислотні властивості.
Алюміній оксид – амфотерний.
Відповідь: B.
ТЕМА: Основні класи неорганічних сполук. Солі. Реакції обміну між електролітами у розчині. Явище амфотерності.
Завдання скеровано на перевірку вміння визначати можливість перебігу реакції обміну між електролітами в розчині.
Якщо в кожну пробірку добавляти краплями водний розчин натрій гідроксиду спочатку в обох пробірках утворяться осади нерозчинних гідроксидів. Магній гідроксид осно́вний, тому з надлишком лугу не реагуватиме. Натомість осад амфотерного алюміній гідроксиду в надлишку лугу розчиниться.
Суть реакцій, що відбулися, можна описати за допомогою скорочених йонних рівнянь:
Відповідь: А.
ТЕМА: Неорганічна хімія. Неорганічні речовини і їхні властивості. Алюміній гідроксид.
Завдання скеровано на перевірку знання властивостей алюміній гідроксиду.
Алюміній хлорид реагує з натрій гідроксидом із утворенням осаду амфотерного алюміній гідроксиду, який здатен розчинятися під дією лугу:
Відповідь: B.
ТЕМА: Неорганічні речовини і їхні властивості. Амфотерність. Алюміній гідроксид.
Завдання скеровано на перевірку розуміння суті амфотерності.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості. З кислотами алюміній гідроксид
Тож для доведення його амфотерності потрібно використати сульфатну кислоту й калій гідроксид:
Відповідь: Г.
ТЕМА: Неорганічні речовини і їхні властивості. Амфотерність.
Завдання скеровано на перевірку розуміння суті амфотерності.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості. Цинк гідроксид реагує як із кислотами, так і з лугами, тобто є амфотерним:
Відповідь: A.
ТЕМА: Неорганічна хімія. Оксид і гідроксид Алюмінію.
Завдання скеровано на перевірку знання властивостей алюміній оксиду й алюміній гідроксиду.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або основні, або кислотні властивості. Оксид і гідроксид Алюмінію реагують як із кислотами, так і з лугами. Тобто є амфотерними:
Алюміній гідроксид за нагрівання розкладається на алюміній оксид і воду:
Відповідь: B.
ТЕМА: Явище амфотерності.
Завдання скеровано на перевірку розуміння суті амфотерності, уміння аналізувати й прогнозувати результати дослідження, робити висновки.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або основні, або кислотні властивості. Наприклад, із кислотами цинк гідроксид реагує як основа, із лугами – як кислота. Тобто білий драглистий осад цинк гідроксиду розчиниться як у кислоті, так і в надлишку розчину лугу.
Описані перетворення можна пояснити за допомогою таких хімічних рівнянь:
Відповідь: B.
ТЕМА: Загальна хімія. Електролітична дисоціація. Реакції йонного обміну між електролітами в розчині.
Завдання скеровано на перевірку вміння перетворювати скорочені йонні рівняння на молекулярні.
Реакції обміну між електролітами в розчинах відбуваються за участю йонів. За умовою завдання мають прореагувати дві розчинні сполуки, одна з яких дисоціює з утворенням катіона Алюмінію, а друга – з утворенням гідроксид-аніона. Умову завдання задовольняють алюміній нітрат і калій гідроксид:
Відповідь: A.
ТЕМА: Загальна хімія. Амфотерність. Алюміній оксид.
Завдання скеровано на перевірку розуміння суті амфотерності.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості.
Амфотерні оксиди під час взаємодії з кислотою або кислотним оксидом виявляють властивості, характерні для основних оксидів. Так само, як основні оксиди, вони взаємодіють з кислотами з утворенням солі і води. У реакціях із лугами або з оксидами лужних і лужноземельних елементів амфотерні оксиди виявляють кислотні властивості.
Відповідь: Г.
ТЕМА: Неорганічні речовини і їхні властивості. Амфотерність. Цинк гідроксид.
Завдання скеровано на перевірку розуміння суті амфотерності.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості. З кислотами цинк гідроксид
Відповідь: Г.





