Розділ: Будова атома і періодична система хімічних елементів
Тема: Протонне число
Кількість завдань: 47
ТЕМА: Загальна хімія. Будова атомів і простих йонів.
Завдання скеровано на перевірку знання складу атома й розуміння причини його електронейтральності, уміння розрізняти атоми і прості йони.
Атом є електрично нейтральною частинкою, що складається з позитивно зарядженого ядра, яке практично визначає його масу (понад 99,9 %), й електронів, що оточують ядро й визначають розміри атома.
Протони й електрони – частинки, заряди яких однакові за абсолютною величиною і протилежні за знаком, нейтрони – електронейтральні.
Простий катіон – це позитивно заряджений йон, одноатомна частинка, що несе на собі один чи більше зарядів протона. Катіон – частинка, на яку перетворюється атом унаслідок утрати одного чи кількох електронів.
Тому для визначення простого катіона потрібно вибрати в таблиці рядок, у якому описано склад частинки з більшою кількістю протонів порівняно з електронами.
Цю умову задовольняє частинка, склад якої описано в рядку Г.
Відповідь: Г.
ТЕМА: Загальна хімія. Будова атомів і простих йонів.
Завдання скеровано на перевірку знання складу атома й розуміння причини його електронейтральності.
Атом є електрично нейтральною частинкою, що складається з позитивно зарядженого ядра, яке практично визначає його масу (понад 99,9 %), й електронів, що оточують ядро й визначають розміри атома.
Протони й електрони – частинки, заряди яких однакові за абсолютною величиною і протилежні за знаком, нейтрони – електронейтральні.
Тому для визначення електронейтральної частинки потрібно вибрати в таблиці рядок, у якому описано склад частинки з однаковою кількістю протонів й електронів.
Цю умову задовольняє частинка, склад якої описано в рядку Б.
Відповідь: Б.
ТЕМА: Загальна хімія. Будова атомів і простих йонів.
Завдання скеровано на перевірку вміння інтерпретувати нуклідні символи атомів і простих йонів.
Нуклід – це різновид атомів або йонів з однаковим масовим числом (кількістю нуклонів) та атомним номером (кількістю протонів).
Нуклідним символом називають символ нукліда елемента, біля якого зазначено атомний номер як лівий підрядковий, а масове число – як лівий надрядковий індекс.
Нуклони – це протони й нейтрони. Кількість нейтронів у ядрі дорівнює різниці між масовим і протонним числами.
Умову завдання задовольняє варіант відповіді Г:
у нукліді
Відповідь: Г.
ТЕМА: Будова атома. Протонне число.
Завдання скеровано на перевірку розуміння фізичного змісту порядкового номера хімічного елемента в періодичній системі.
Порядковий номер хімічного елемента в періодичній системі дорівнює його протонному числу й, відповідно, заряду ядра атома. У цьому полягає фізичний зміст порядкового номера хімічного елемента в періодичній системі.
Порядкові номери Натрію і Калію в періодичній системі й, відповідно, їхні протонні числа становлять
Відповідь: Г.
ТЕМА: Будова атома. Протонне число.
Завдання скеровано на перевірку розуміння фізичного змісту порядкового номера хімічного елемента в періодичній системі.
Порядковий номер хімічного елемента в періодичній системі дорівнює його протонному числу й, відповідно, заряду ядра атома. У цьому полягає фізичний зміст порядкового номера хімічного елемента в періодичній системі.
У завданні йдеться про бінарну сполуку Магнію
Умову завдання задовольняє магній оксид
Відповідь: Г.
ТЕМА: Загальна хімія. Періодичний закон і періодична система хімічних елементів.
Завдання скеровано на перевірку розуміння фізичного змісту порядкового номера хімічного елемента в періодичній системі.
Умову завдання задовольняє пара елементів
Відповідь: B.
ТЕМА: Будова атома. Протонне число.
Завдання скеровано на перевірку розуміння фізичного змісту порядкового номера хімічного елемента в періодичній системі.
Порядковий номер хімічного елемента в періодичній системі дорівнює його протонному числу й, відповідно, заряду ядра атома. У цьому полягає фізичний зміст порядкового номера хімічного елемента в періодичній системі.
Відповідь: B.
ТЕМА: Будова атома. Протонне число. Поширеність хімічних елементів у земній корі.
Завдання скеровано на перевірку знання поширеності хімічних елементів у земній корі та вміння визначати протонне число хімічного елемента за його місцем у періодичній системі.
Найпоширенішими хімічними елементами земної кори є Оксиген і Силіцій. Їхні порядкові номери в періодичній системі
Відповідь: 22.
ТЕМА: Загальна хімія. Закономірності періодичної системи хімічних елементів.
Завдання скеровано на перевірку вміння аналізувати будову атома за місцем хімічного елемента в періодичній системі.
В атомах хімічних елементів VIIА групи зі збільшенням протонного числа збільшується кількість енергетичних рівнів. Флуор, Хлор, Бром, Йод, Астат – елементи другого, третього, четвертого, п’ятого, шостого періодів відповідно, а номер періоду дорівнює кількості енергетичних рівнів в атомі.
Відповідь: Г.
ТЕМА: Будова атома. Протонне число.
Завдання скеровано на перевірку вміння визначати будову зовнішнього енергетичного рівня атома хімічного елемента та його протонне число за місцем у періодичній системі.
Сім електронів на зовнішньому енергетичному рівні міститься в атомах хімічних елементів VIIА групи – галогенів. Умову завдання задовольняє елемент із протонним числом
Відповідь: B.
ТЕМА: Загальна хімія. Будова атомів і простих йонів.
Завдання скеровано на перевірку вміння інтерпретувати нуклідні символи атомів і простих йонів.
Йон – позитивно (катiон) або негативно (анiон) електрично заряджена частинка, заряд якої кратний заряду електрона.
Тобто за умовою завдання потрібно визначити частинку, у якій кількість електронів більша за кількість протонів. Цій умові відповідає варіант відповіді A – у цій частинці кількість електронів на два більша за кількість протонів.
Відповідь: A.
ТЕМА: Загальна хімія. Будова атома.
Завдання перевіряє знання понять «нуклонне число», «нуклід», «протонне число», «нейтрони».
Для виконання завдання необхідно знати, як за положенням елемента в періодичній системі визначити число протонів, нейтронів, нуклонне число. Нуклонне число – це відносна атомна маса. За умовою завдання – 48. Протонне число визначається порядковим номером хімічного елемента, у Титана порядковий номер – 22. Нейтронне число (кількість нейтронів) визначається різницею між відносною атомною масою і порядковим номером: 48 – 22 = 26.
Отже, правильна відповідь – Г.
Відповідь: Г.
ТЕМА: Основні хімічні поняття. Будова атома.
Завдання скеровано на перевірку вміння аналізувати будову атомів хімічних елементів.
Нуклід – це різновид атомів або йонів з однаковим масовим числом (кількість нуклонів) та атомним номером (кількістю протонів).
Нуклідним символом називають символ нукліда елемента, біля якого зазначено атомний номер як лівий підрядковий, а масове число – як лівий надрядковий індекс.
Нуклони – це протони й нейтрони.
Протонне число
Кількість нейтронів
Порядковий номер Кобальту в періодичній системі – 27, тобто
Масове (нуклонне) число Кобальту – 59, тобто
Тож можна обчислити кількість нейтронів у ядрі нукліда

Відповідь: Г.
ТЕМА: Будова атома. Склад атомних ядер. Поняття нуклід, нуклонне і протонне число, число нейтронів.
Завдання перевіряє знання протонного і нуклонного чисел, уміння визначати за протонним і нуклонним числами число нейтронів.
Нуклонне число (А) – відносна атомна маса, протонне число (Z) – порядковий номер елемента. Число нейтронів (N) визначається як різниця між нуклонним і протонним числами. Отже, у нукліда Ферум-56,
Відповідь: A.
ТЕМА: Загальна хімія. Протонне число. Електронна будова атомів і простих йонів.
Завдання скеровано на перевірку вміння аналізувати будову атомів і простих йонів.
| Хімічний символ | Порядковий номер у періодичній системі | Протонне число | Кількість електронів |
| 19 | 19 | ||
| 18 (19 – 1) | |||
| 20 | 20 (18 + 2) | ||
В атомі невідомого елемента
Відповідь: 20.
ТЕМА: Загальна хімія. Будова атома. Енергетичні рівні й підрівні.
Завдання скеровано на перевірку вміння визначати кількість енергетичних рівнів в електронній оболонці атомів.
Номер періоду, у якому міститься хімічний елемент, збігається з кількістю енергетичних рівнів у його електронній оболонці.
Тобто умову завдання задовольняє пара хімічних елементів, що належать до одного періоду. Їхні протонні числа –
| Хімічний елемент | |||
| Протонне число | Символ | Номер періоду | Кількість енергетичних рівнів в атомі |
| 7 | 2 | ||
| 8 | 2 | ||
| 15 | 3 | ||
| 16 | 3 | ||
| 33 | 4 | ||
Відповідь: A.
ТЕМА: Основні хімічні поняття. Будова атома.
Завдання скеровано на перевірку вміння аналізувати будову атомів хімічних елементів.
Нуклід – це різновид атомів або йонів з однаковим масовим числом (кількість нуклонів) та атомним номером (кількістю протонів).
Нуклідним символом називають символ нукліда елемента, біля якого зазначено атомний номер як лівий підрядковий, а масове число – як лівий надрядковий індекс.
Нуклони – це протони й нейтрони. Нейтронне число
Якщо кількість протонів і нейтронів однакова, то нуклонне число є парним, тобто вибір потрібно зробити між нуклідами
Кількість нейтронів у нукліді
Відповідь: Б.
ТЕМА: Загальна хімія. Будова атома. Протонне число.
Завдання скеровано на перевірку вміння визначати протонне число хімічного елемента за його місцем у періодичній системі.
Кількість протонів в атомі дорівнює номеру хімічного елемента в періодичній системі.
Порядкові номери Магнію і Кальцію в періодичній системі
Відповідь: 32.
ТЕМА: Загальна хімія. Будова атома. Протонне число.
Завдання скеровано на перевірку вміння визначати будову атома за місцем хімічного елемента в періодичній системі.
За кількістю електронів на зовнішньому енергетичному рівні можна дійти висновку, що йдеться про хімічний елемент ІІІА (13) групи. Тобто формула його гідроксиду
Відносна атомна маса елемента ІІІА (13) групи Алюмінію –
Його порядковий номер і, відповідно, протонне число, –
Відповідь: Б.
ТЕМА: Періодичний закон і періодична система хімічних елементів. Будова атома.
Завдання скеровано на перевірку вміння визначати протонне число й будову зовнішнього енергетичного рівня атома за місцем хімічного елемента в періодичній системі.
За умовою в атомі хімічного елемента шість електронів на зовнішньому енергетичному рівні. Тобто це елемент 6А (16) групи періодичної системи.
Умову завдання з-поміж наведених задовольняє елемент із протонним числом 16 Сульфур.
Відповідь: Б.
ТЕМА: Періодичний закон і періодична система хімічних елементів. Будова атома.
Завдання скеровано на перевірку розуміння фізичного змісту порядкового номера хімічного елемента в періодичній системі, уміння визначати протонне число елемента.
Порядковий номер Літію в періодичній системі, а отже і його протонне число, дорівнює трьом.
Відповідь: B.
ТЕМА: Періодичний закон і періодична система хімічних елементів. Будова атома.
Завдання скеровано на перевірку вміння визначати протонне число хімічного елемента за його місцем у періодичній системі.
У четвертому періоді VІ групі побічній підгрупі міститься Хром. Його порядковий номер 24, тож і протонне число цього хімічного елемент – 24.
Відповідь: Б.
ТЕМА: Періодичний закон і періодична система хімічних елементів. Металічні й неметалічні елементи. Будова атома.
Завдання скеровано на перевірку вміння аналізувати структуру періодичної системи хімічних елементів.
У періодах зі збільшенням атомних мас металічний характер елементів послаблюється, а неметалічний – посилюється.
А
Б
В
Г
Нітроген
Відповідь: Б.
ТЕМА: Періодична система хімічних елементів.
Завдання скеровано на перевірку вміння визначати місце елемента в періодичній системі.
Хімічний елемент V A групи, розташований у ІV періоді, – Арсен.
Його порядковий номер у періодичній системі – 33. Тож і протонне число Арсену дорівнює 33.
Відповідь: B.
ТЕМА: Періодична система хімічних елементів.
Завдання скеровано на перевірку вміння визначати природу хімічного елемента за його положенням у періодичній системі.
Протонне число хімічного елемента збігається з його номером у періодичній системі.
Лужноземельні елементи належать до ІІ А групи, із-поміж наведених цю умову задовольняє добірка
| Протонні числа | Хімічні символи | |
| A | 3; 11; 55 | |
| Б | 5; 13; 49 | |
| B | 17; 35; 53 | |
| Г | 20; 38; 56 |
Відповідь: Г.
ТЕМА: Загальна хімія. Будова атомів. Періодична система хімічних елементів. Хімічний зв’язок.
Завдання скеровано на перевірку вміння аналізувати будову атомів хімічних елементів, визначати тип хімічного зв’язку в речовині за її формулою.
Протонні числа атомів хімічних елементів збігаються з їхніми номерами в періодичній системі, тобто йдеться про бінарну сполуку Калію з Бромом – калій бромід, формула якого
Калій – типовий металічний, а Бром – типовий неметалічний елемент. Атом Калію легко втрачає електрон зовнішнього енергетичного рівня й перетворюється на однозарядний катіон. Атом Брому легко приймає електрон для завершення зовнішнього енергетичного рівня і перетворюється на однозарядний аніон. Хімічний зв'язок між катіоном й аніоном – йонний.
Відповідь: Г.
ТЕМА: Загальна хімія. Будова атомів. Періодична система хімічних елементів.
Завдання скеровано на перевірку вміння аналізувати будову атомів хімічних елементів, визначати формулу гідрату оксиду хімічного елемента за місцем елемента в періодичній системі.
Оскільки в атомі хімічного елемента на зовнішньому енергетичному рівні три електрони, можна дійти висновку, що це елемент ІІІ А підгрупи. Тобто хімічна формула його гідроксиду
Відносна атомна маса 27 в Алюмінію, його протонне число 13.
Відповідь: Б.
ТЕМА: Кристалічні ґратки. Будова речовини.
Завдання скеровано на перевірку вміння аналізувати хімічну формулу й визначати тип кристалічних ґраток у речовині.
Протонні числа хімічних елементів збігаються з їхніми протонними числами. У завданні йдеться про воду (протонне число Гідрогену 1, Оксигену – 8). Кристалічні ґратки у воді молекулярні – у їхніх вузлах містяться її молекули.
Відповідь: A.
ТЕМА: Кристалічні ґратки. Будова речовини.
Завдання скеровано на перевірку вміння аналізувати хімічну формулу й визначати тип кристалічних ґраток у речовині.
Протонні числа хімічних елементів збігаються з їхніми протонними числами. У завданні йдеться про калій флуорид (протонне число Калію 19, Флуору – 9). Це типові металічний і неметалічний елементи з великою різницею електронегативності. Тому в цій речовині утворення хімічного зв’язку пов’язане з переходом електрона від атома Калію до атома Флуору. Між катіоном Калію і флуорид-аніоном, що утворилися, виникає йонний зв’язок. Тож кристалічні ґратки в цій речовині йонні.
Відповідь: A.
ТЕМА: Загальна хімія. Будова речовини. Кристалічні ґратки. Йонний зв’язок.
Завдання скеровано на перевірку розуміння змісту поняття кристалічні ґратки, уміння прогнозувати тип кристалічних ґраток у речовині за її хімічною формулою.
Протонне число 9 в елемента Флуору, 11 – у Натрію, тобто в завданні йдеться про натрій флуорид.
Йонний зв’язок – це зв’язок між катіонами й аніонами. Його можна розглядати як граничний випадок ковалентного полярного зв’язку. Якщо різниця в значеннях електронегативності атомів хімічних елементів дуже велика (рис. 1), спільні електронні пари практично повністю зміщуються до атома більш електронегативного елемента. За цих умов атоми перетворюються на йони (рис. 2).
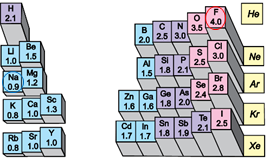
Рис. 1. Відносна електронегативність атомів хімічних елементів
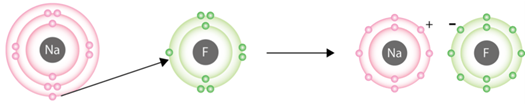
Рис. 2. Утворення йонів Натрію і Флуору
Кристалічні ґратки – модель, за допомогою якої описують внутрішню будову кристалів. Точки кристалічних ґраток, у яких розташовані частинки, називають вузлами кристалічних ґраток. Природа частинок у вузлах кристалічних ґраток та сили взаємодії між частинками визначають тип ґраток: атомні, молекулярні, йонні.
Йонні кристали утворюють більшість солей неорганічних і органічних кислот, луги, основні й амфотерні оксиди й гідроксиди.
У кристалічних ґратках натрій флуориду містяться катіони Натрію і флуорид-аніони, тобто кристалічні ґратки в натрій флуориді йонні.
Відповідь: B.
ТЕМА: Основні хімічні поняття. Будова атома.
Завдання скеровано на перевірку вміння аналізувати будову атомів хімічних елементів.
Нуклід – це різновид атомів або йонів з однаковим масовим числом (кількість нуклонів) та атомним номером (кількістю протонів).
Нуклідним символом називають символ нукліда елемента, біля якого зазначено атомний номер як лівий підрядковий, а масове число – як лівий надрядковий індекс.
Нуклони – це протони й нейтрони. Нейтронне число
Якщо кількість протонів і нейтронів однакова, то нуклонне число є парним, тобто вибір потрібно зробити між нуклідами
| Нуклідний символ | ||||
| A | 12 | 6 | 6 | |
| Б | 18 | 8 | 10 | |
| B | 21 | 10 | 11 | |
| Г | 22 | 10 | 12 |
Відповідь: A.
ТЕМА: Загальна хімія. Будова атомів і простих йонів.
Завдання скеровано на перевірку розуміння змісту понять атом, катіон, аніон, протон, електрон, уміння аналізувати склад атомів і простих йонів.
Аніони – негативно заряджені частинки, на які перетворюються атоми внаслідок приєднання електронів. Однозарядний аніон Брому утворюється внаслідок приєднання електрона до атома Брому, кількість протонів в атомі не змінюється:
Катіони – позитивно заряджені частинки, на які перетворюються атоми внаслідок утрачання електронів. Тризарядний катіон Алюмінію утворюється внаслідок утрачання трьох електронів атомом Алюмінію, кількість протонів в атомі не змінюється:
| Частинка | Протонне число | Кількість електронів | |
| A | атом Алюмінію | 13 | 13 |
| Б | атом Брому | 35 | 35 |
| B | катіон Алюмінію | 13 | 10 |
| Г | аніон Брому | 35 | 36 |
Відповідь: Г.
ТЕМА: Періодична система хімічних елементів.
Завдання скеровано на перевірку вміння визначати формули леткої сполуки хімічного елемента з Гідрогеном, вищого оксиду і його гідрату за положенням елемента в періодичній системі.
Хімічний елемент із протонним числом 16 – Сульфур, формула гідроген сульфіду
Відповідь: B.
ТЕМА: Загальна хімія. Будова атома. Кількість електронів на зовнішньому енергетичному рівні в атомі.
Завдання скеровано на перевірку вміння визначати кількість електронів на зовнішньому енергетичному рівні в атомі.
Кількість електронів на зовнішньому енергетичному рівні в атомі, визначають за номером групи (короткоперіодна форма періодичної системи), у якій розташований хімічний елемент у періодичній системі.
Протонне число хімічного елемента дорівнює його порядковому номеру в періодичній системі.
Тобто потрібно визначити пару хімічних елементів тієї самої групи. З-поміж наведених це елементи з протонними числами
Відповідь: B.
ТЕМА: Загальна хімія. Будова атома. Кількість енергетичних рівнів в атомі.
Завдання скеровано на перевірку вміння визначати кількість енергетичних рівнів в атомі за його місцем у періодичній системі.
Кількість енергетичних рівнів, на яких містяться електрони в атомі, визначають за номером періоду, у якому розташований хімічний елемент у періодичній системі.
Протонне число хімічного елемента дорівнює його порядковому номеру в періодичній системі.
Тобто потрібно визначити пару хімічних елементів того самого періоду. З-поміж наведених це елементи з протонними числами
Відповідь: A.
ТЕМА: Будова атома. Протонне число.
Завдання скеровано на перевірку вміння визначати будову зовнішнього енергетичного рівня атома хімічного елемента та його протонне число за місцем у періодичній системі.
Три електрони на зовнішньому енергетичному рівні міститься в атомах хімічних елементів IIІА групи. Умову завдання задовольняє елемент із протонним числом
Відповідь: B.
ТЕМА: Обчислення в хімії. Визначення формули речовини за даними щодо місця одного з хімічних елементів – її складників – у періодичній системі.
Завдання скеровано на перевірку вміння визначати формулу речовини за даними щодо місця одного з хімічних елементів – її складників – у періодичній системі.
Дано:
Знайти:
Відповідь: 15.
ТЕМА: Загальна хімія. Будова атома. Протонне число.
Завдання скеровано на перевірку вміння визначати протонні числа хімічних елементів.
Протонне число збігається з порядковим номером хімічного елемента в періодичній системі.
| Хімічний елемент | ||
| Символ | Порядковий номер у періодичній системі (протонне число) |
|
| 20 | Б | |
| 25 | A | |
| 26 | B | |
| 29 | Г | |
Відповідь: Б А В Г.
ТЕМА: Загальна хімія. Характеристика хімічного елемента за його місцем у періодичній системі.
Завдання скеровано на перевірку вміння прогнозувати властивості хімічних елементів за їхнім місцем у періодичній системі.
Елемент із протонним числом
Умову завдання задовольняє речовина, формула якої
Відповідь: Б.
ТЕМА: Загальна хімія. Періодична система хімічних елементів. Протонне число.
Завдання скеровано на перевірку вміння визначати протонне число хімічного елемента за його місцем у періодичній системі.
Протонне число хімічного елемента дорівнює порядковому номеру елемента в періодичній системі.
| Символ хімічного елемента | Порядковий номер у періодичній системі | Протонне число | |
| B | 7 | ||
| Б | 20 | ||
| Г | 25 | ||
| A | 34 | ||
Відповідь: В Б Г А.
ТЕМА: Загальна хімія. Будова атома.
Завдання скеровано на перевірку вміння визначати будову атома хімічного елемента.
Формула вищого оксиду елемента ІV групи –
Тобто йдеться про Титан, його порядковий номер у періодичній системі хімічних елементів і, відповідно, протонне число дорівнює
Відповідь: A.
ТЕМА: Будова атома. Протонне число.
Завдання скеровано на перевірку вміння визначати будову зовнішнього енергетичного рівня атома хімічного елемента та його протонне число за місцем у періодичній системі.
Два електрони на зовнішньому енергетичному рівні міститься в атомах хімічних елементів IIА групи. Умову завдання задовольняє елемент із протонним числом
Відповідь: Б.
ТЕМА: Неорганічна хімія. Неметалічні елементи. Неметали. Озон. Хлор.
Завдання скеровано на перевірку знання галузей застосування неметалів.
Найпоширенішими дезінфектантами води на водопровідних станціях є хлор й озон. Протонні числа Хлору й Оксигену –
Відповідь: 25.
ТЕМА: Загальна хімія. Закономірності періодичної системи хімічних елементів.
Завдання скеровано на перевірку вміння аналізувати будову атома за місцем хімічного елемента в періодичній системі.
В атомах хімічних елементів другого періоду послідовно збільшуються номери груп, до яких вони належать, і, відповідно, кількість електронів на зовнішньому енергетичному рівні їхніх атомів.
Відповідь: Г.
ТЕМА: Загальна хімія. Будова атома. Протонне число.
Завдання скеровано на перевірку вміння визначати будову зовнішнього енергетичного рівня атома хімічного елемента та його протонне число за місцем у періодичній системі.
П’ять електронів на зовнішньому енергетичному рівні міститься в атомах хімічних елементів VА групи. Умову завдання задовольняє елемент із протонним числом
Відповідь: Б.
ТЕМА: Періодичний закон і періодична система хімічних елементів. Будова атома.
Завдання скеровано на перевірку вміння визначати протонне число хімічного елемента за його місцем у періодичній системі.
У четвертому періоді VІІ групі головній підгрупі міститься Бром. Його порядковий номер 35, тож і протонне число цього хімічного елемент – 35.
Відповідь: Г.
ТЕМА: Періодичний закон і періодична система хімічних елементів. Металічні й неметалічні елементи.
Завдання скеровано на перевірку вміння аналізувати структуру періодичної системи хімічних елементів.
На початку кожного періоду (окрім першого) лужний елемент, наприкінці – інертний.
У періодах зі збільшенням атомних мас металічний характер елементів послаблюється, а неметалічний – посилюється.
Побічні підгрупи утворені елементами лише великих періодів. Усі ці елементи – металічні.
А
Б
В
Г
Натрій – лужний елемент, Берилій – металічний елемент, Ферум – металічний елемент (рис. 1).
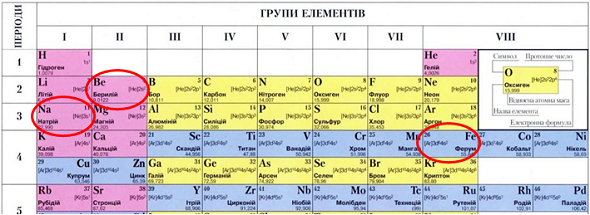
Відповідь: Б.





