Розділ: Розв’язування задач за рівняннями реакцій
Тема: Розв’язування задач за рівняннями реакцій: комбіновані задачі
Кількість завдань: 108
ТЕМА: Гідрування алкінів. Обчислення масової частки речовини в суміші.
Завдання скеровано на перевірку знання хімічних формул вуглеводнів, розуміння суті реакцій гідрування, уміння обчислювати склад суміші.
Бут-1-ин і бут-2-ин є ізомерами й мають молекулярну формулу
Збільшення маси після реакції становить
Кількість речовини водню:
Бутин
Молярна маса бутину:
Маса бутинів:
Маса бутану в початковій суміші:
Масова частка бутану в початковій суміші:
Відповідь: 19.
ТЕМА: Оксиди елементів другої групи періодичної таблиці. Хімічні властивості оксидів.
Завдання скеровано на перевірку знання властивостей оксидів елементів другої групи й уміння обчислювати масові співвідношення за хімічними рівняннями.
Рівняння хімічної реакції оксиду
Маса середньої солі втричі більша за масу оксиду, тобто:
Кількість речовини оксиду така сама, що й кількість речовини середньої солі:
Відповідно молярна маса середньої солі втричі більша за молярну масу оксиду:
Молярна маса середньої солі:
Молярна маса оксиду:
За умовою
Отже,
Молярна маса оксиду:
Відповідь: 40.
ТЕМА: Обчислення в хімії. Обчислення за хімічними рівняннями. Розв’язування комбінованих задач.
Завдання скеровано на перевірку вміння розв’язувати комбіновані розрахункові задачі.
Оскільки калій гідроксид був у надлишку, приріст маси відбувся внаслідок реакції з вуглекислим газом:
Обчислімо об’єм (н. у.) вуглекислого газу кількістю речовини
Обчислімо об’ємну частку вуглекислого газу в суміші:
Відповідь: 25.
ТЕМА: Обчислення в хімії. Обчислення за хімічними рівняннями. Визначення хімічної формули речовини. Естери. Естерифікація.
Завдання скеровано на перевірку вміння розв’язувати розрахункові задачі з визначення формули спирту за даними щодо мас реактантів і продукту в реакції естерифікації.
У реакції естерифікації реактантами є спирт і карбонова кислота, продукти реакції – естер і вода:
Згідно із законом збереження маси обчислімо масу води:
Обчислімо кількість речовини води як частку від ділення її маси на молярну масу:
Кількості речовини спирту, карбонової кислоти, естеру, води однакові і становлять
Молярна маса спирту дорівнює частці від ділення його маси на кількість речовини:
Відповідь: 60.
ТЕМА: Обчислення в хімії. Суміші. Обчислення масової частки
Завдання скеровано на перевірку вміння розв’язувати розрахункові задачі за хімічними рівняннями.
За рівнянням
Кисень у надлишку, тому після повного окиснення чадного газу до вуглекислого об’єм кисню зменшиться на
Унаслідок повного окиснення чадного газу об’ємом
Сумарний об’єм газової суміші після реакції:
Об’ємна частка кисню в цій суміші:
Відповідь: 60.
ТЕМА: Обчислення в хімії. Обчислення за хімічними рівняннями маси продукту, якщо один із реактантів у надлишку. Відносний вихід продукту реакції.
Завдання скеровано на перевірку вміння розв’язувати розрахункові задачі за хімічними рівняннями.
За рівнянням
Кисень у надлишку, обчислюємо масу магній оксиду, що утворився, за масою магнію, який у реакції витратиться повністю:
Відповідь: 6.
ТЕМА: Обчислення в хімії. Вираження кількісного складу розчину (суміші).
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Розв’язання
Із хлоридною кислотою реагують і магній гідроксид, і магній карбонат, однак карбон(IV) оксид утворюється лише внаслідок реакції з магній карбонатом:
Відповідь: 10.
ТЕМА: Обчислення в хімії. Обчислення маси продукту реакції за його відносним виходом і масою реагенту, що містить домішки.
Завдання скеровано на перевірку вміння аналізувати й обчислювати кількісний склад розчинів.
Дано:
Знайти:
Розв’язання
Відповідь: 69.
ТЕМА: Обчислення в хімії. Обчислення складу суміші.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Розв’язання
Відповідь: 341.
ТЕМА: Обчислення в хімії. Обчислення відносного виходу речовини.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Розв’язання
Відповідь: 75.
ТЕМА: Обчислення в хімії. Обчислення за хімічними рівняннями.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Розв’язання
Відповідь: 65.
ТЕМА: Обчислення в хімії. Обчислення за хімічними рівняннями.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Розв’язання
Відповідь: 29.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі за рівняннями хімічних реакцій.
Дано:
Знайти:
Відповідь: 30.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі за рівняннями хімічних реакцій.
Дано:
Знайти:
За умовою задачі
За рівнянням реакції:
Відповідь: 18.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Молярні маси етану й метаналю однакові – 30 г/моль.
Відповідь: 40.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 400.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 20.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння визначати молекулярну формулу речовини за її масою і масами продуктів її повного окиснення.
Дано:
Знайти:
Найпростіша формула речовини -
Відповідь: 8.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 30.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Якщо маса етену в суміші
Якщо внаслідок згоряння етену масою
За рівнянням реакції
Відповідь: 20.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 32.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння визначати хімічну формулу сполуки.
Дано:
Знайти:
Тобто
Відповідь: 12.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Для газів об'ємні частки в суміші збігаються з мольними, тому
Відповідь: 80.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння визначати хімічну формулу сполуки.
Дано:
Знайти:
Відповідь: 14.
ТЕМА: Обчислення в хімії. Розв’язування задач за рівняннями реакцій.
Завдання скеровано на перевірку вміння розв’язувати розрахункові задачі на визначення складу суміші.
1. За умовою задачі об’єм газуватої суміші становив 50 мл. Нехай
2. Записуємо рівняння реакцій горіння метану й етану. За рівнянням (1) і (2) реакцій відповідно до закону об’ємних відношень газів визначаємо об’єм карбон(ІV) оксиду в кожній реакції.
3. Загальний об'єм карбон(ІV) оксиду, що утворився, становить 60 мл.
Складаємо алгебричне рівняння і розв'язуємо його:
Відповідь: 10.
ТЕМА: Обчислення в хімії. Розв’язування задач за рівняннями реакцій.
Завдання скеровано на перевірку вміння здійснювати розрахунки за рівняннями хімічних реакцій.
У водному розчині карбонати перетворюються на гідрогенкарбонати.
1) обчислюємо об’єм карбон(ІV) оксиду, який прореагував з карбонатами:
2) записуємо рівняння реакцій, унаслідок яких карбонати перетворюються на гідрогенкарбонати:
Нехай під час повного перетворення у водному розчині карбонатів на гідрогенкарбонати в реакцію (1) вступає карбон(ІV) оксид кількістю речовини х моль , тоді в реакцію (2) – карбон(ІV) оксид кількістю речовини (0,1 – х) моль.
3) за умовою задачі маса суміші карбонатів становила 9,2 г.
Складаємо алгебричне рівняння й обчислюємо
Відповідь: 5.
ТЕМА: Обчислення в хімії. Розв'язування задач за рівняннями реакцій.
Завдання скеровано на перевірку вміння обчислювати за рівнянням хімічної реакції відносний вихід продукту реакції.
Для виконання завдання необхідно розуміти, як здійснювати розрахунки за рівняннями оборотних реакцій.
1) за рівнянням реакції визначаємо мольні співвідношення реагентів:
З азоту кількістю речовини 1 моль утворюється амоніак кількістю речовини 2 моль, тому з азоту об’ємом 25 л утворився амоніак об’ємом 50 л:
2) за умовою задачі відносний вихід амоніаку становить 20 %, обчислюємо практичний об’єм амоніаку:
3) за рівнянням хімічної реакції обчислюємо об’єми азоту і водню, які витратили на добування 10 л амоніаку:
4) обчислюємо об’єм азоту, який залишився після реакції, й об’єм суміші після реакції:
5)
Відповідь: 20.
ТЕМА: Органічна хімія. Вуглеводні. Метан. Хімічні властивості метану. Об’ємні відношення газів під час хімічних реакцій
Завдання скеровано на перевірку знання хімічних властивостей метану й уміння прогнозувати продукти реакцій за його участі.
Об’ємне, а отже й мольне відношення, метану й хлору, узятих для реакції, становлять
Відповідь: B.
ТЕМА: Обчислення в хімії. Обчислення за хімічним рівнянням кількості речовини газуватого продукту за відомою масою реагенту й масовою часткою домішок у ньому.
Завдання скеровано на перевірку вміння обчислювати за хімічним рівнянням кількості речовини газуватого продукту за відомою масою реагенту й масовою часткою домішок у ньому.
Дано:
Знайти:
Відповідь: 2.
ТЕМА: Обчислення в хімії. Обчислення за хімічним рівнянням об’єму газуватого реагенту за відомою масою іншого реагенту.
Завдання скеровано на перевірку вміння обчислювати за хімічним рівнянням об’єм газуватого реагенту за відомою масою продукту реакції та його відносним виходом.
Дано:
Знайти:
Відповідь: 112.
ТЕМА: Обчислення в хімії. Обчислення за хімічними рівняннями. Комбіновані задачі.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
За рівнянням реакції
Відповідь: 84.
ТЕМА: Обчислення в хімії. Комбіновані задачі. Визначення складу суміші.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 2.
ТЕМА: Обчислення в хімії. Обчислення відносного виходу продукту реакції.
Завдання скеровано на перевірку вміння обчислювати відносний вихід продукту реакції.
Дано:
Знайти:
Відповідь: 80.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 40.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 60.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння обчислювати масу (об’єм) розчину й розчинника; масу й масову частку розчиненої речовини.
Дано:
Знайти:
Відповідь: 845.
ТЕМА: Обчислення в хімії. Розв’язування задач за рівняннями реакцій.
Завдання перевіряє вміння розв’язувати розрахункові задачі на визначення складу суміші.
За умовою завдання до суміші порошків магнію і заліза добавили хлоридну кислоту. І магній, і залізо реагують з хлоридною кислотою з утворенням солей і виділенням водню.
1) напишемо рівняння реакцій взаємодії металів з кислотою:
За рівняннями реакцій кількість речовини металів така сама, як і кількість водню. Нехай кількість речовини водню, який виділяється в реакції (1), дорівнює х моль, тоді кількість речовини водню, який виділяється в реакції (2), дорівнює
2) виразимо маси металів через
3) обчислюємо масу заліза і його масову частку в суміші:
Відповідь: 70.
ТЕМА: Обчислення в хімії. Розв’язування задач за рівняннями реакцій.
Завдання перевіряє вміння розв’язувати розрахункові задачі за рівняннями хімічних реакцій.
1) проаналізуємо, які речовини суміші будуть реагувати з хлоридною кислотою, узятою в надлишку. Із двох речовин суміші (магній і силіцій) з хлоридною кислотою буде реагувати лише магній, унаслідок цієї взаємодії виділяється водень:
2) обчислимо кількість моль водню, який виділився під час хімічної реакції:
3) за рівнянням реакції взаємодії магнію з хлоридною кислотою, якщо виділяється 0,25 моль водню, то і магнію вступає в реакцію 0,25 моль. Обчислюємо кількість магнію і його масу:
4) обчислюємо масову частку магнію в суміші:
Відповідь: 30.
ТЕМА: Обчислення в хімії. Розв’язування задач за рівняннями реакцій
Завдання перевіряє вміння розв’язувати розрахункові задачі за рівняннями хімічних реакцій.
1) обчислимо масу сульфатної кислоти у вихідному розчині:
2) обчислимо масу сульфур(VI) оксиду, який добавили до розчину кислоти:
3) під час змішування сульфур(VI) оксиду з розчином кислоти, оксид реагує з водою, яка є в розчині, з утворенням сульфатної кислоти. Обчислимо масу сульфатної кислоти, яку можна отримати з 2 моль сульфур(VI) оксиду:
4) обчислимо загальну масу сульфатної кислоти в утвореному розчині:
5) обчислимо масу розчину, який утворився після змішування сульфур(VI) оксиду з розчином кислоти:
6) обчислимо масову частку сульфатної кислоти в утвореному розчині:
Відповідь: 61.
ТЕМА: Обчислення в хімії.
Завдання перевіряє вміння розв’язувати комбіновані задачі, обчислювати кількісний склад суміші.
Для виконання завдання необхідно знати хімічні властивості органічних речовин. Бромідна кислота реагує з амінами, але не реагує з алканами. Унаслідок згоряння алканів утворюються вуглекислий газ і вода, а метиламіну – вуглекислий газ, вода й азот.
За умовою завдання загальна кількість речовини
За рівнянням (1)
Відповідь: 50.
ТЕМА: Обчислення в хімії.
Завдання перевіряє вміння робити розрахунки, коли під час змішування суміші з водою відбувається хімічна реакція.
Для виконання завдання необхідно з умови зрозуміти, що олеум – це суміш сульфур(VI) оксиду та безводної сульфатної кислоти, а для добування розчину сульфатної кислоти змішують олеум з водою. Під час змішування сульфур(VI) оксид реагує з водою з утворенням сульфатної кислоти.
Відповідь: 645.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 4.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння обчислювати масу (об’єм) розчину й розчинника; масу й масову частку розчиненої речовини.
Дано:
Знайти:
За рівнянням реакції
Відповідь: 64.
ТЕМА: Обчислення в хімії. Масова частка компонента в суміші. Розв’язування задач за рівняннями реакцій.
Завдання перевіряє вміння визначати за рівняннями хімічних реакцій масу речовини в суміші і обчислювати масову частку цієї речовини в суміші.
Для виконання завдання необхідно вміти проводити розрахунки за рівняннями хімічних реакцій і розуміти що означає масова частка речовини в суміші.
1) за умовою задачі в реакції відновлення вступає водень кількістю речовини
2) за рівняннями реакцій визначаємо кількість речовини, а за формулами масу та масову частку купрум(І) оксиду в суміші:
Відповідь: 90.
ТЕМА: Обчислення в хімії. Вираження кількісного складу розчину (суміші).
Завдання перевіряє вміння обчислювати об’ємну частку речовини в суміші.
Для виконання завдання необхідно знати хімічні властивості насичених вуглеводнів і амінів і вміти розраховувати об’ємну частку речовини в суміші.
1) унаслідок пропускання суміші, що складається з етану та етанаміну, крізь склянку з бромідною кислотою, маса склянки збільшується, тому що етанамін реагує з бромідною кислотою. На скільки збільшилася маса склянки, стільки етанаміну вступає в реакцію, тобто
2) обчислюємо кількість етанаміну:
3) обчислюємо об’єм етанаміну:
4) обчислюємо об’ємну частку етанаміну в суміші:
Відповідь: 40.
ТЕМА: Обчислення в хімії. Вираження кількісного складу розчину (суміші). Розв’язування задач за рівняннями реакцій.
Завдання перевіряє вміння обчислювати масову частку розчиненої речовини в розчині та розв’язувати задачі за рівнянням хімічної реакції.
Для виконання завдання необхідно знати хімічні властивості оснóвних оксидів і вміти розраховувати масову частку речовини за масою з рівняння хімічної реакції.
1) Обчислюємо масу літій гідроксиду у вихідному розчині:
2) Обчислюємо масу літій оксиду, який добавили до розчину:
3) Обчислюємо масу утвореного розчину лугу:
4) Якщо до розчину літій гідроксиду добавити літій оксид, то між літій оксидом і водою, яка є в розчині, відбувається хімічна реакція. За реакцією визначаємо кількість, а після цього масу літій гідроксиду, який утворився із літій оксиду:
5) Обчислюємо масу літій гідроксиду в утвореному розчині:
6) Обчислюємо масову частку літій гідроксиду в розчині, що утворився:
Відповідь: 10.
ТЕМА: Обчислення в хімії. Обчислення за хімічним рівнянням. Розв’язування комбінованих задач.
Завдання скеровано на перевірку вміння розв’язувати за хімічними рівняннями комбіновані задачі.
Дано:
Знайти:
Відповідь: 186.
ТЕМА: Обчислення в хімії. Розв’язування комбінованих задач.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 81.
ТЕМА: Обчислення в хімії. Обчислення відносного виходу продукту реакції.
Завдання скеровано на перевірку вміння обчислювати відносний вихід продукту реакції.
Дано:
Знайти:
Відповідь: 95.
ТЕМА: Обчислення в хімії. Визначення формули речовини за кількісними даними щодо продуктів реакції за її участі.
Завдання скеровано на перевірку вміння визначати формулу речовини за кількісними даними щодо продуктів реакції за її участі.
Дано:
Знайти:
Протонне число Калію і його порядковий номер у періодичній системі хімічних елементів –
Відповідь: 19.
ТЕМА: Органічна хімія. Вуглеводні. Алкани. Хімічні властивості алканів.
Завдання скеровано на перевірку вміння аналізувати рівняння реакцій, що властиві алканам.
За умовою завдання
Рівняння реакції хлорування метану таке:
Відповідь: Б.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 30.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння визначати молекулярну формулу речовини за її масою і масами продуктів її повного окиснення.
Дано:
Знайти:
Найпростіша формула речовини –
Відповідь: 8.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
За рівнянням реакції
Відповідь: 42.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 70.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння визначати масу продукту реакції за відомими масою реагенту й масовою часткою чистої речовини в ньому.
Дано:
Знайти:
Відповідь: 21.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 42.
ТЕМА: Обчислення в хімії. Обчислення відносного виходу продукту реакції.
Завдання скеровано на перевірку вміння обчислювати відносний вихід продукту реакції.
Дано:
Знайти:
Відповідь: 75.
ТЕМА: Обчислення в хімії. Обчислення масової частки складника суміші. Комбіновані задачі.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 10.
ТЕМА: Обчислення в хімії. Виведення молекулярної формули речовини.
Завдання скеровано на перевірку вміння виводити молекулярну формулу речовини за даними щодо продуктів її згоряння і відносною густиною пари.
Дано:
Знайти:
Відповідь: 12.
ТЕМА: Обчислення в хімії. Обчислення масової частки складника в суміші.
Завдання скеровано на перевірку вміння обчислювати масову частку складника в суміші.
Дано:
Знайти:
Відповідь: 65.
ТЕМА: Обчислення в хімії. Обчислення за хімічними рівняннями.
Завдання скеровано на перевірку вміння обчислювати за хімічними рівняннями масу продукту реакції, якщо один з реагентів узято в надлишку.
Дано:
Знайти:
За рівнянням реакції
У реакції повністю витратиться барій нітрат, сульфатна кислота в надлишку.
Відповідь: 233.
ТЕМА: Обчислення в хімії. Обчислення за хімічними рівняннями.
Завдання скеровано на перевірку вміння обчислювати практичну масу продукту реакції за відомою кількістю речовини реагенту й відносним виходом продукту.
Дано:
Знайти:
Відповідь: 492.
ТЕМА: Обчислення в хімії. Виведення молекулярної формули речовини за даними щодо продуктів його згоряння і відносною густиною його пари за іншим газом.
Завдання скеровано на перевірку вміння виводити формулу вуглеводню за даними щодо продуктів його згоряння і відносною густиною його пари за іншим газом.
Дано:
Знайти:
Відповідь: 8.
ТЕМА: Обчислення в хімії. Обчислення маси реагенту за відомою масою і відносним виходом продукту реакції.
Завдання скеровано на перевірку вміння обчислювати масу реагенту за відомою масою і відносним виходом продукту реакції.
Дано:
Знайти:
Відповідь: 100.
ТЕМА: Обчислення в хімії. Визначення масової частки реагенту в суміші за відомим об’ємом газуватого продукту реакції.
Завдання скеровано на перевірку вміння обчислювати масову частку реагенту в суміші за відомим об’ємом газуватого продукту реакції.
Дано:
Знайти:
Відповідь: 40.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Знайти:
Відповідь: 30.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 208.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 8.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння обчислювати масу хімічного елемента в речовині за її кількістю.
Дано:
Знайти:
Відповідь: 85.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 40.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
1. Знайти:
2. Знайти:
Відповідь: 1. 84. 2. 18.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
1. Знайти:
2. Знайти:
Відповідь: 1. 88. 2. 20.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння обчислювати масову частку розчиненої речовини.
Дано:
Знайти:
Відповідь: 118.
ТЕМА: Обчислення в хімії. Комбіновані задачі.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 29
ТЕМА: Обчислення в хімії. Обчислення об’єму продукту реакції між газуватими речовинами, якщо одну з них узято в надлишку.
Завдання скеровано на перевірку вміння розв’язувати задачі з обчислення об’єму продукту реакції між газуватими речовинами, якщо одну з них узято в надлишку.
Дано:
Знайти:
Кисень у надлишку – із метаном об'ємом 8 л прореагує кисень об'ємом 16 л, а для реакції взято кисень об'ємом 20 л.
Відповідь: 8.
ТЕМА: Обчислення в хімії. Комбіновані задачі.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 40.
ТЕМА: Обчислення в хімії. Комбіновані задачі.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 81.
ТЕМА: Обчислення в хімії. Комбіновані задачі.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 70.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 50.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння визначати масу продукту реакції за відомими масою реагенту й масовою часткою чистої речовини в ньому.
Дано:
Знайти:
Відповідь: 486.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 30.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння обчислювати маси / об’єми реагентів і продуктів реакцій за хімічними рівняннями.
Дано:
1. Знайти:
2. Знайти:
Відповідь: 1. 2240. 2. 4480.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння виводити молекулярну формулу речовини.
Дано:
1. Знайти:
2. Знайти:
Відповідь: 1. 56. 2. 12.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння обчислювати масову частку розчиненої речовини.
Дано:
Знайти:
Відповідь: 50.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 72.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння виводити молекулярну формулу речовини.
Дано:
1. Знайти:
2. Знайти:
Відповідь: 1. 56. 2. 16.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Маса склянки з бромною водою збільшилася за рахунок реакції брому з етином:
Відповідь: 48.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння обчислювати за хімічним рівнянням масу продукту реакції, якщо один із реагентів узято в надлишку.
Дано:
Знайти:
За рівнянням реакції
Тобто ортофосфатна кислота в надлишку. З натрій гідроксидом кількістю речовини
Тому з ортофосфатною кислотою кількістю речовини
Відповідь: 41.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння обчислювати відносний вихід продукту реакції.
Дано:
Знайти:
Відповідь: 50.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
1. Знайти:
2. Знайти:
Ізомери складу
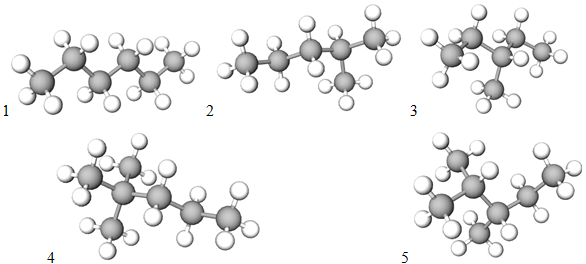
Рис. 1. Ізомери складу
Відповідь: 1. 20. 2. 5.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Маса склянки з хлоридною кислотою збільшилася за рахунок реакції гідрогенхлориду з етаміном:
Відповідь: 6720.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння обчислювати за хімічним рівнянням масу продукту реакції, якщо один із реагентів узято в надлишку.
Дано:
Знайти:
За рівнянням реакції
Тобто сульфатна кислота в надлишку. З натрій гідроксидом кількістю речовини
Маса середньої солі, яка не прореагувала, дорівнює
Відповідь: 71.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 5.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 48.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння обчислювати масову частку хімічного елемента в речовині за її формулою.
Дано:
Знайти:
Відповідь: 45.
ТЕМА: Обчислення в хімії. Обчислення за хімічними рівняннями відносного виходу продукту реакції за об’ємом газуватого реагенту.
Завдання скеровано на перевірку вміння обчислювати відносний вихід продукту реакції за об’ємом газуватого реагенту.
Дано:
Знайти:
Відповідь: 80.
ТЕМА: Обчислення в хімії. Обчислення за хімічними рівняннями. Масова частка розчиненої речовини.
Завдання скеровано на перевірку вміння обчислювати масу реагенту за відомою масою іншого реагенту й маси розчину за масовою часткою розчиненої речовини.
Дано:
Знайти:
Відповідь: 16.
ТЕМА: Обчислення в хімії. Визначення складу суміші.
Завдання скеровано на перевірку вміння визначати склад суміші.
Дано:
Знайти:
Відповідь: 73.
ТЕМА: Обчислення в хімії. Обчислення за хімічними рівняннями. Комбіновані задачі.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 1.
ТЕМА: Обчислення в хімії. Обчислення відносного виходу продукту реакції.
Завдання скеровано на перевірку вміння обчислювати відносний вихід продукту реакції.
Дано:
Знайти:
Відповідь: 80.
ТЕМА: Обчислення в хімії. Обчислення за хімічними рівняннями об’єму газуватого реагенту за відомим об’ємом іншого газуватого реагенту, що містить домішки.
Завдання скеровано на перевірку вміння обчислювати за хімічним рівнянням об’єму газуватого реагенту за відомим об’ємом іншого газуватого реагенту, що містить домішки.
Дано:
Знайти:
Відповідь: 14.
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння визначати формулу речовини за масами продуктів її згоряння і відносною густиною за іншим газом.
Дано:
Знайти:
Відповідь: 6.
ТЕМА: Обчислення в хімії. Обчислення за хімічними рівняннями. Комбіновані задачі.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
За рівнянням реакції
Відповідь: 42.
ТЕМА: Обчислення в хімії. Обчислення за хімічними рівняннями.
Завдання скеровано на перевірку вміння обчислювати масу продукту реакції за хімічним рівнянням, якщо один із реагентів узято в надлишку.
Дано:
Знайти:
За рівнянням реакції
Відповідь: 42.
ТЕМА: Обчислення в хімії. Обчислення за хімічними рівняннями. Комбіновані задачі.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 95.
ТЕМА: Обчислення в хімії. Обчислення за хімічними рівняннями.
Завдання скеровано на перевірку вміння обчислювати масу продукту реакції за хімічним рівнянням, якщо один із реагентів узято в надлишку.
Дано:
Знайти:
Відповідь: 10.
ТЕМА: Обчислення в хімії. Обчислення за хімічними рівняннями.
Завдання скеровано на перевірку вміння обчислювати масу продукту реакції за відомим об’ємом газуватого реагенту й виходом продукту від теоретичного.
Дано:
Знайти:
Відповідь: 828.





