НМТ онлайн 2026 року з хімії – демоваріант
Демонстраційний варіант національного мультитесту (НМТ) 2026 року з хімії
ТЕМА: Основні хімічні поняття. Речовина.
Щоб визначити правильну відповідь, треба взяти до уваги дві умови одночасно:
1) молекула має бути триатомною, тобто складатися з трьох атомів;
2) речовина має бути складною, тобто утвореною атомами різних хімічних елементів.
Перевірмо варіанти:
A \(\mathrm{CH_2O}\) – у молекулі \(4\) атоми;
Б \(\mathrm{NH_3}\) – у молекулі \(4\) атоми;
B \(\mathrm{CO_2}\) – у молекулі \(3\) атоми \((1\ \mathrm{C}\ \text{і}\ 2\ \mathrm{O})\) двох хімічних елементів, отже речовина складна;
Г \(\mathrm{O_3}\) – у молекулі \(3\) атоми одного хімічного елемента \((\mathrm{O})\), тому це проста речовина, а не складна.
Отже, єдина речовина, що відповідає обом вимогам, – вуглекислий газ, формула якого \(\mathrm{CO_2}.\)
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Періодичний закон і періодична система хімічних елементів. Будова атомів і простих йонів.
У ряду Флуор → Хлор → Бром → Йод (збільшення протонних чисел у групі галогенів):
- радіус атома збільшується (додаються електронні шари);
- електронегативність зменшується (ядро слабше притягує зовнішні електрони ядро).
Отже, правильне поєднання: радіус атома збільшується, електронегативність зменшується.
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Хімічний зв'язок. Типи кристалічних ґраток.
Зображено модель кристалічних ґраток, де кожна кулька – це атом, а з’єднання між ними – хімічні зв’язки. Така структура характерна для речовин з атомними кристалічними ґратками, де всі атоми зв’язані між собою в єдину тривимірну сітку.
Розгляньмо варіанти:
А йод – має молекулярні ґратки;
Б лід – молекулярні ґратки (молекули \(\mathrm{H_2O}\));
В метан – молекулярна речовина;
Г алмаз – атомні кристалічні ґратки, де всі атоми Карбону зв’язані міцними однаковими ковалентними зв’язками
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Суміші речовин. Розчини.
Зображено побутовий глечик-роздільник, який має носик у нижній частині, що дає змогу злити рідину знизу, залишаючи жир, який спливає нагору. Це пристрій механічного розділення за принципом різної густини речовин.
Розгляньмо варіанти:
А розділити столовий оцет на кислоту й воду зображеним пристроєм не можна, потрібна фракційна дистиляція.
Б відокремити рідкий жир від м’ясного бульйону зображеним пристроєм можна, рідкий жир і м’ясний бульйон не змішуються, жир спливає вгору, бульйон зливають через носик.
В розділити рідкий жир на гліцерол і жирні кислоти зображеним пристроєм не можна, потрібна хімічна реакція гідролізу, не механічне розділення.
Г відокремити етиловий спирт від метилового зображеним пристроєм не можна, потрібна фракційна дистиляція.
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Суміші речовин. Розчини. Неорганічні речовини і їхні властивості.
У завданні описано три водні розчини з однаковою кількістю речовини \((0{,}05\ \text{моль})\) у воді об’ємом \(1\ \text{л}{:}\)
\(\mathrm{NH_3}\) (амоніак) – водний розчин має слабкі основні властивості, \(\mathrm{pH}\approx 10–11.\)
\(\mathrm{H_2S}\) (сірководень) – водний розчин має слабкі кислі властивості, \(\mathrm{pH}\approx 4–5.\)
\(\mathrm{HCl}\) (гідроген хлорид) – водний розчин є сильною кислотою, \(\mathrm{pH}\approx 1.\)
\(\mathrm{pH}\) – це показник кислотності розчину.
Розташувавши розчини речовин за зростанням \(\mathrm{pH}\), маємо:
\begin{gather*} \xrightarrow[\mathrm{pH}\ \text{зростає}]{\mathrm{HCl\rightarrow H_2S\rightarrow NH_3}}. \end{gather*}Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Хімічна реакція. Поняття окисник, відновник, окиснення, відновлення.
Визначмо, у яких реакціях Нітроген відновлюється (тобто є окисником).
Окисник приймає електрони й відновлюється (ступінь окиснення зменшується).
Реакція 1
\begin{gather*} \mathrm{CuO+NH_3\rightarrow Cu+N_2+H_2O}. \end{gather*}Ступінь окиснення Нітрогену в \(\mathrm{NH_3}\) \(-3\), а в \(\mathrm{N_2}\) ступінь його окиснення \(0\), тобто вищий. Отже \(\mathrm{N}\) окиснюється, \(\mathrm{NH_3}\) відновник. Нітроген тут не окисник.
Реакція 2
\begin{gather*} \mathrm{Cu+N_2O\rightarrow N_2+CuO}. \end{gather*}Ступінь окиснення Нітрогену в \(\mathrm{N_2O{:}\ +1}\), а в \(\mathrm{N_2\ –\ 0}\), тобто зменшується, отже \(\mathrm{N}\) відновлюється, а \(\mathrm{N_2O}\) – окисник, Нітроген у ньому окисник.
Реакція 3
\begin{gather*} \mathrm{NO+O_2\rightarrow NO_2}. \end{gather*}Ступінь окиснення Нітрогену \(\mathrm{N}\) підвищується з \(+2\) до \(+4\), отже \(\mathrm{N}\) окиснюється, Нітроген в \(\mathrm{NO}\) відновник.
Реакція 4
\begin{gather*} \mathrm{N_2+H_2\rightarrow NH_3}. \end{gather*}Ступінь окиснення Нітрогену зменшується від \(0\) до \(–3\), отже \(\mathrm{N}\) відновлюється, Нітроген в \(\mathrm{N_2}\) окисник.
Отже, Нітроген є окисником у реакціях 2 (у складі \(\mathrm{N_2O}\)) і 4 (у складі \(\mathrm{N_2}\)).
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Хімічна реакція. Хімічна рівновага, принцип Ле Шательє.
Рівняння електролітичної дисоціації етанової кислоти:
\begin{gather*} \mathrm{CH_3COOH\rightleftarrows CH_3COO^-+H^+}. \end{gather*}Щоб змістити рівновагу праворуч (у напрямку дисоціації кислоти на йони), треба зменшити концентрацію одного з продуктів, наприклад катіонів \(\mathrm{H^+}.\)
Проаналізуймо варіанти відповіді.
А хлоридна кислота \((\mathrm{HCl})\) дисоціює, унаслідок цього підвищується концентрація катіонів \(\mathrm{H^+}\), рівновага зміщується вліво.
Б натрій хлорид \((\mathrm{NaCl})\) – середня сіль, її дисоціація не впливає на концентрацію \(\mathrm{H^+}\), рівновага не зміститься.
В натрій гідроксид \((\mathrm{NaOH})\) – сильна основа, дисоціює з утворенням гідроксид-іонів, які зв’язують \(\mathrm{H^+}{:}\)
\begin{gather*} \mathrm{NaOH\rightarrow Na^++OH^-};\\[7pt] \mathrm{H^++OH^-\rightarrow H_2O}. \end{gather*}Зменшення концентрації йонів \(\mathrm{H^+}\) сприяє зміщенню рівноваги праворуч.
Г Метанова кислота \((\mathrm{HCOOH})\) дисоціює, що підвищує концентрацію \(\mathrm{H^+}\) і сприяє зміщенню рівноваги вліво.
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Загальні відомості про металічні елементи та метали. Ряд активності металів.
Щоб, за надлишку розведеної хлоридної кислоти, сплав прореагував лише частково, у ньому має бути метал, що реагує, і метал, що не реагує з хлоридною кислотою.
Скориставшись рядом активності металів, визначаємо, що водень з хлоридної кислоти не витісняють мідь \((\mathrm{Cu})\) і срібло \((\mathrm{Ag}).\)
Умові завдання відповідає лише варіант В \((\mathrm{Zn}\), \(\mathrm{Cu}){:}\) складник сплаву цинк прореагує з хлоридною кислотою, а мідь – ні.
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Сполуки неметалічних елементів із Гідрогеном.
Оцінімо можливість перебігу реакцій між газами за нормальних умов:
А метан і гідроген сульфід не реагують один з одним.
Б метан й амоніак не реагують один з одним
В гідроген хлорид й амоніак реагують миттєво, утворюючи білий дим амоній хлориду:
\begin{gather*} \mathrm{HCl\ (\text{газ})\ + NH_3\ (\text{газ})\ \rightarrow NH_4Cl\ (\text{твердий})}. \end{gather*}Г гідроген хлорид і гідроген сульфід не реагують один з одним.
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Найважливіші сполуки Алюмінію. Явище амфотерності. Хімічні властивості, способи добування амфотерних оксидів і гідроксидів.
Алюміній може бути складником катіонів солей:
\begin{gather*} \mathrm{Al^{3+}Cl_3^-{;}\ Al^{3+}(NO_3)_3^-{;}\ Al_2^{3+}(SO_4)_3^{2-}}. \end{gather*}Алюміній може бути складником аніонів солей:
\begin{gather*} \mathrm{Na^+[Al^{3+}(OH)_4^-]{;}\ K^+[Al^{+3}(OH)_4^-]{;}\ Na^+(Al^{+3}O_2^{-2})^-}. \end{gather*}Алюміній оксид реагує з хлоридною кислотою:
\begin{gather*} \mathrm{Al_2O_3+6HCl=2AlCl_3+3H_2\uparrow}. \end{gather*}Алюміній оксид реагує з натрій гідроксидом:
\begin{gather*} \mathrm{Al_2O_3+2NaOH+3H_2O\rightarrow 2Na[Al(OH)_4]}{;}\\[7pt] \mathrm{Al_2O_3+2NaOH\xrightarrow{\text{стоплення}} 2NaAlO_2+H_2O}. \end{gather*}Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Кислоти. Основність кислот.
Одноосновна кислота – це кислота, молекула якої містить один атом Гідрогену, здатний до заміщення (наприклад, \(\mathrm{HCOOH}\), \(\mathrm{HNO_3}\), \(\mathrm{HCl}\)).
Проаналізуймо варіанти:
А \(\mathrm{FeSO_4}\) – сіль сульфатної кислоти \(\mathrm{H_2SO_4}\) (двоосновної).
Б \(\mathrm{FePO_4}\) – сіль ортофосфатної кислоти \(\mathrm{H_3PO_4}\) (триосновної).
В \(\mathrm{NH_4HCO_3}\) – гідрогенкарбонат, сіль двоосновної кислоти \(\mathrm{H_2CO_3}.\)
Г \(\mathrm{HCOONH_4}\) – сіль метанової (мурашиної) кислоти \(\mathrm{HCOOH}\), яка є одноосновною.
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Солі. Хімічні властивості солей.
Відповідно до умови завдання треба, щоб реакції відбулися в обох пробірках, а осад утворився лише в одній.
А \(\mathrm{KNO_3}\) – реакції не відбуваються.
Б \(\mathrm{BaCl_2}\)
\begin{gather*} \mathrm{BaCl_2+Na_2CO_3=BaCO_3\downarrow +\ 2NaCl};\\[7pt] \mathrm{BaCl_2+Na_2SiO_3\rightarrow BaSiO_3\downarrow+2NaCl}. \end{gather*}Осад утворюється в обох пробірках.
B \(\mathrm{Ca(OH)_2}\)
\begin{gather*} \mathrm{Ca(OH)_2+Na_2CO_3\rightarrow CaCO_3\downarrow +\ 2NaOH};\\[7pt] \mathrm{Ca(OH)_2+Na_2SiO_3\rightarrow CaSiO_3\downarrow +\ 2NaOH}. \end{gather*}Осад утворюється в обох пробірках.
Г \(\mathrm{HCl}\)
\begin{gather*} \mathrm{Na_2CO_3+2HCl\rightarrow 2NaCl+CO_2\uparrow +\ H_2O}\ \text{(реакція є, осаду немає)};\\[7pt] \mathrm{Na_2SiO_3+2HCl\rightarrow 2NaCl+ H_2SiO_3\downarrow}\ \text{(утворюється осад)}. \end{gather*}Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Властивості алканів, алкенів, спиртів. Типи хімічних реакцій в органічній хімії.
Розгляньмо перетворення:
\(\mathrm{C_2H_6\rightarrow C_2H_4}\) – відщеплення \(\mathrm{H_2}\) – дегідрування (варіант відповіді А);
\(\mathrm{C_2H_4\rightarrow C_2H_5OH}\) – приєднання води – гідратація (варіант відповіді В);
\(\mathrm{C_2H_5OH\rightarrow CH_3COOC_2H_5}\) (за участю \(\mathrm{CH_3COOH}\)) – естерифікація (варіант відповіді Г).
Поміж реакцій, які відбулися, немає реакції гідрування (варіант відповіді Б).
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Ізомерія і хімічні властивості алкенів.
Маємо речовину, формула якої \(\mathrm{(CH_3)_2=CH_2}\) – це 2-метилпроп-1-ен (ізобутен).
I. Структурним ізомером речовини є бут-2-ен.
Обидві речовини мають формулу \(\mathrm{C_4H_8}\), але різну будову (розгалужений і нерозгалужений алкени).
II. Назва речовини – 1,1-диметилетен.
Правильна систематична назва – 2-метилпроп-1-ен, а не 1,1-диметилетен.
III. Речовина вступає в реакцію полімеризації.
Це алкен, має подвійний зв’язок, може полімеризуватися:
\begin{gather*} n\mathrm{(CH_3)_2C=CH_2\rightarrow (\text{-}(CH_3)_2CCH_2\text{-})}n. \end{gather*}IV. Каталітичним гідруванням речовини можна добути 2-метилбутан.
Продуктом гідрування є 2-метилпропан (ізобутан), а не 2-метилбутан:
\begin{gather*} \mathrm{(CH_3)_2C=CH_2+H_2\rightarrow (CH_3)_2CH-CH_3}. \end{gather*}Отже, правильні лише твердження I і твердження III.
Відповідь: A.
Знайшли помилку? Пишіть на
ТЕМА: Бензен.
А продуктом окиснення фенолу є оксигеновмісна речовина
Б продуктами ізомеризації гексану є ізомерні алкани
В бензен можна добути тримеризацією етину:
\begin{gather*} \mathrm{3CH\equiv CH\rightarrow C_6H_6} \end{gather*}Г продуктом гідрування циклогексану є гексан
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Карбонові кислоти. Етанова кислота.
Описана речовина добре розчинна у воді, має різкий запах і кислий смак, її використовують у кулінарії як приправу й консервант.
Це чітко вказує на оцтову кислоту (етанову кислоту, \(\mathrm{CH_3COOH}\)).
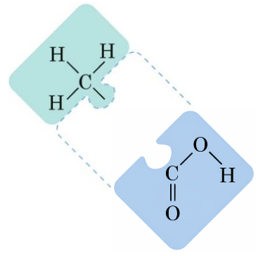
На зображенні – фрагмент молекули \(\mathrm{\text{-}CH_3}\), тобто метильна група.
Щоб скласти формулу оцтової кислоти, треба додати карбоксильну групу \(\mathrm{\text{-}COOH}.\)
Відповідь: A.
Знайшли помилку? Пишіть на
ТЕМА: Вуглеводи. Гідроліз дисахаридів.
Під час утворення дисахариду з двох молекул моносахариду відщеплюється молекула води:
\begin{gather*} \mathrm{C_6H_{12}O_6+C_6H_{12}O_6-H_2O=C_{12}H_{22}O_{11}}. \end{gather*}У молекулі мальтози \(22\) атоми Гідрогену.
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Аміни. Анілін. Етанол. Фенол. Метанова й етанова кислоти.
А Анілін – слабша основа, ніж амоніак, бо електронну пару \(\mathrm{{:}N}\) втягнуто в бензенове кільце.
Б Метанамін \(\mathrm{(CH_3NH_2)}\) – сильніша основа, ніж метанамін, бо метильна група підвищує електронну густину на атомі Нітрогену.
В Фенол виявляє сильніші кислотні властивості, ніж етанол, бо фенол легше відщеплює протон \(\mathrm{H^+}.\)
Г Метанова кислота \(\mathrm{(HCOOH)}\) сильніша за оцтову.
Фенол справді має сильніші кислотні властивості, ніж етанол. Це єдине правильне твердження серед запропонованих.
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Якісні реакції органічних і неорганічних сполук.
Утворення 1 (розчину синього кольору) є наслідком реакції, що відбулася після Б (змішування розчину гліцеролу зі свіжоосадженим купрум(ІІ) гідроксидом за надлишку лугу).
Утворення 2 (блискучого шару металу на стінках посудини) є наслідком реакції, що відбулася після В (змішування розчину метаналю з амоніачним розчином аргентум(І) оксиду й нагрівання).
Утворення 3 (вибухонебезпечного газу) є наслідком реакції, що відбулася після А (занурення магнієвої стрічки у водний розчин метанової кислоти).
Відповідь: 1Б, 2В, 3А.
Знайшли помилку? Пишіть на
ТЕМА: Гідроліз солей.
А \(\mathrm{KCl}\) – сіль сильної кислоти і сильної основи, середовище водного розчину нейтральне.
Б \(\mathrm{AlCl_3}\) – сіль сильної кислоти і слабкої основи у водному розчині зазнає гідролізу за катіоном, середовище розчину кисле.
В \(\mathrm{Na_2S}\) – сіль сильної основи і слабкої кислоти у водному розчині зазнає гідролізу за аніоном, середовище розчину лужне.
Г \(\mathrm{ZnSO_4}\) – сіль слабкої основи і сильної кислоти у водному розчині зазнає гідролізу за катіоном, середовище розчину кисле.
Д \(\mathrm{K_3PO_4}\) – сіль сильної основи і слабкої кислоти у водному розчині зазнає гідролізу за аніоном, середовище розчину лужне.
Тепер підставляємо у твердження.
1. Середовище водного розчину солі … – нейтральне.
Єдина сіль із-поміж зазначених, водний розчин якої нейтральний, калій хлорид \(\mathrm{KCl}.\) Отже, 1 – A.
2. У водному розчині відбувається гідроліз за аніоном солей Д та …
Гідроліз за аніоном мають солі слабких кислот:
Д \(\mathrm{K_3PO_4}\) – гідроліз за аніоном \(\mathrm{PO_4^{3-}}{;}\)
В \(\mathrm{Na_2S}\) – гідроліз за аніоном \(\mathrm{S^{2-}}.\)
Отже, 2 – B.
3. Метилоранж набуває рожевого забарвлення у водних розчинах солей Б та …
Рожевий колір метилового оранжевого свідчить про кисле середовище. Кисле середовище мають розчини солей слабких основ і сильних кислот:
Б \(\mathrm{AlCl_3}\) – кисле середовище;
Г \(\mathrm{ZnSO_4}\) – також кисле середовище.
Отже, 3 – Г.
Відповідь: 1А, 2В, 3Г.
Знайшли помилку? Пишіть на
ТЕМА: Алкани. Відносна молекулярна маса. Ізомерія алканів.
1. Молекулярна формула 2 метилбутану \(\mathrm{C_5H_{12}}.\)
\begin{gather*} M_r\mathrm{(C_5H_{12})=5\cdot 12+12\cdot 1=72}. \end{gather*}Відповідь: \(72.\)
2. Молекулярна формула 2-метилбутану \(\mathrm{C_5H_{12}}.\)
Їй відповідають три структурні ізомери: (пентан, 2 метилбутан, 2,2 диметилпропан).
Тобто 2-метилбутан має два структурні ізомери: пентан і 2,2-диметилпропан.
Відповідь: \(2.\)
Відповідь: 1. \(72.\) 2. \(2.\)
Знайшли помилку? Пишіть на
ТЕМА: Розчини. Розчинність. Кількісний склад розчинів.
За графіком визначаємо, що за температури \(90\ ^\circ\mathrm{C}\) у воді масою \(100\) г розчиняється натрій йодид масою \(300\) г.
Обчислюємо масову частку натрій йодиду в розчині:
\begin{gather*} w\mathrm{(NaI)}=\frac{m\mathrm{(NaI)}}{m\mathrm{(NaI)}+m\mathrm{(H_2O)}};\\[6pt] w\mathrm{(NaI)}=\frac{300\ \text{г}}{300\ \text{г}+100\ \text{г}};\\[6pt] w\mathrm{(NaI)}=\frac{300\ \text{г}}{400\ \text{г}};\\[6pt] w\mathrm{(NaI)}=0{,}75\ (\text{або}\ 75\ \%). \end{gather*}Відповідь: \(75.\)
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії.
Рівняння реакції синтезу амоніаку:
\begin{gather*} \mathrm{N_2+3H_2\rightarrow 2NH_3}. \end{gather*}За рівнянням:
\begin{gather*} 1\ \text{об'єм}\ \mathrm{N_2}+3\ \text{об'єми}\ \mathrm{H_2}\rightarrow 2\ \text{об'єми}\ \mathrm{NH_3}. \end{gather*}Водню взято \(600\) л.
Амоніаку синтезовано \(60\) л.
Теоретичний вихід:
згідно з рівнянням \(3\ \text{об'єми}\ \mathrm{H_2}\rightarrow 2\ \text{об'єми}\ \mathrm{NH_3}.\)
Тобто
\begin{gather*} V_\text{теор.}\mathrm{(NH_3)}=\frac 23 V\mathrm{(H_2)}=\frac 23\cdot 600\ \text{л}=400\ \text{л}. \end{gather*}Відносний вихід амоніаку:
\begin{gather*} \varphi\mathrm{(NH_3)}=\frac{V_\text{практ.}\mathrm{(NH_3)}}{V_\text{теор.}\mathrm{(NH_3)}}=\frac{60\ \text{л}}{400\ \text{л}}=0{,}15\ (\text{або}\ 15\ \%). \end{gather*}Відповідь: \(15.\)
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії.
У суміші два складники: \(\mathrm{CaCO_3}\) i \(\mathrm{KHCO_3}.\)
Маса однієї порції суміші – \(m\) г.
Перша порція суміші реагує з калій гідроксидом \(\mathrm{KOH}\) масою \(56\) г, друга – з нітратною кислотою \(\mathrm{HNO_3}\) масою \(189\) г.
1. Реакція з \(\mathrm{KOH}.\)
Реагує тільки калій гідрогенкарбонат:
\begin{gather*} \mathrm{KHCO_3+KOH\rightarrow K_2CO_3+H_2O.} \end{gather*}Молярна маса \(\mathrm{KOH}{:}\)
\begin{gather*} M(\mathrm{KOH})=56\ \text{г/моль}\Rightarrow n(\mathrm{KOH})=\frac{56\ \text{г}}{56\ \text{г/моль}}=1\ \text{моль}. \end{gather*}Отже,
\begin{gather*} n\mathrm{(KHCO_3)}=1\ \text{моль};\\[7pt] M\mathrm{(KHCO_3)}=100\ \text{г/моль};\\[7pt] m\mathrm{(KHCO_3)}=1\ \text{моль}\cdot 100\ \text{г/моль}=100\ \text{г}. \end{gather*}2. Реакція з \(\mathrm{HNO_3}.\)
Реагують обидві речовини:
\begin{gather*} \mathrm{CaCO_3+2HNO_3\rightarrow Ca(NO_3)_2+CO_2+H_2O};\\[7pt] \mathrm{KHCO_3+HNO_3\rightarrow KNO_3+CO_2+H_2O};\\[7pt] M\mathrm{(HNO_3)}=63\ \text{г/моль};\\[6pt] n\mathrm{(HNO_3)}=\frac{189\ \text{г}}{63\ \text{г/моль}}=3\ \text{моль}; \end{gather*}Позначмо:
- \(n_1\) – кількість речовини \(\mathrm{CaCO_3}{;}\)
- \(n_2\) – кількість речовини \(\mathrm{KHCO_3};\)
\(n_2=1\ \text{моль}.\)
Кількість \(\mathrm{HNO_3}\), що витрачається:
\begin{gather*} 2n_1+n_2=3;\\[7pt] 2n_1+1=3;\\[7pt] 2n_1=2;\\[7pt] n_1=1\ \text{моль}. \end{gather*}Тоді:
\begin{gather*} m\mathrm{(CaCO_3)}=1\ \text{моль}\cdot 100\ \text{г/моль}=100\ \text{г}. \end{gather*}3. Маса однієї порції суміші
\begin{gather*} m=m\mathrm{(CaCO_3)}+m\mathrm{(KHCO_3)}=100\ \text{г}+100\ \text{г}=200\ \text{г}. \end{gather*}Відповідь: \(200.\)
Знайшли помилку? Пишіть на




