ЗНО онлайн 2014 року з хімії – основна сесія
Тестові завдання основної сесії ЗНО 2014 року з хімії
ТЕМА: Основні хімічні поняття. Фізичні явища і хімічні реакції.
Завдання скеровано на перевірку вміння розрізняти фізичні явища і хімічні реакції.
Суттєвою ознакою хімічного явища є перетворення речовин.
Під час випаровування води й плавлення льоду та сама речовина змінює свій агрегатний стан. Подрібнення крейди також не приводить до утворення нових речовин.
Унаслідок згоряння деревини, головним складником якої є целюлоза, утворюються карбон(IV) оксид і вода. Тобто відбувається хімічна реакція.
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Основні хімічні поняття. Склад атома.
Завдання скеровано на перевірку вміння аналізувати склад атомів.
Порядковий номер Оксигену в періодичній системі – 8. Його протонне число – 8, відповідно в ядрі атома Оксигену 8 протонів, а навколо ядра – 8 електронів.
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Періодична система хімічних елементів.
Завдання скеровано на перевірку вміння визначати природу хімічного елемента за його положенням у періодичній системі.
| Символи хімічних елементів | ||
| металічних | неметалічних | |
| A | ||
| Б | ||
| B | ||
| Г | ||
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Основні хімічні поняття. Речовина. Хімічна формула.
Завдання скеровано на перевірку вміння аналізувати хімічну формулу речовини.
Хімічна формула – умовний запис її якісного й кількісного складу за допомогою хімічних символів й індексів.
Молекулярна формула етанової кислоти
У ній записано символи трьох хімічних елементів – Карбону
Праві підрядкові індекси біля хімічних символів у формулі показують кількість атомів відповідного хімічного елемента. Тобто в молекулі етанової кислоти два атоми Карбону, чотири атоми Гідрогену й два атоми Оксигену – у сумі вісім атомів.
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Хімічний зв’язок. Будова речовини.
Завдання скеровано на перевірку вміння аналізувати хімічні формули й розпізнавати йонні сполуки.
Йонний зв’язок – зв’язок між йонами. Формули лише йонних сполук наведено в рядку Г. Кожна із цих сполук утворена катіонами металічних й аніонами неметалічних елементів. Утворення йонного зв’язку можливе за значної різниці в електронегативності хімічних елементів, коли електрони від атомів металічних елементів переходять до атомів неметалічних, унаслідок чого утворюються катіони й аніони.
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Періодична система хімічних елементів.
Завдання скеровано на перевірку вміння визначати місце елемента в періодичній системі.
Леткі сполуки з Гідрогеном складу
Його порядковий номер у періодичній системі – 15.
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Кристалічні ґратки. Будова речовини.
Завдання скеровано на перевірку вміння аналізувати хімічну формулу й визначати тип кристалічних ґраток у речовині.
Протонні числа хімічних елементів збігаються з їхніми протонними числами. У завданні йдеться про калій флуорид (протонне число Калію 19, Флуору – 9). Це типові металічний і неметалічний елементи з великою різницею електронегативності. Тому в цій речовині утворення хімічного зв’язку пов’язане з переходом електрона від атома Калію до атома Флуору. Між катіоном Калію і флуорид-аніоном, що утворилися, виникає йонний зв’язок. Тож кристалічні ґратки в цій речовині йонні.
Відповідь: A.
Знайшли помилку? Пишіть на
ТЕМА: Генетичні зв’язки між класами неорганічних сполук.
Завдання скеровано на перевірку вміння встановлювати генетичні зв’язки між неорганічними сполуками різних класів.
Газ, що утворюється внаслідок дії рідини
Водень є продуктом реакції між хлоридною кислотою (
Відповідь: A.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Реакції обміну між електролітами у водному розчині.
Завдання скеровано на перевірку вміння застосовувати знання про умови необоротності перебігу реакцій обміну між електролітами в розчині.
Реакції обміну між електролітами в розчинах відбуваються за участю йонів. Умови необоротності перебігу реакцій обміну між електролітами в розчині наведено на схемі (рис. 1).
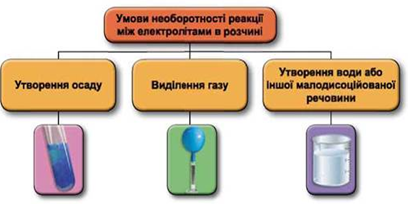
Рис. 1. Умови необоротності реакцій між електролітами у водних розчинах
У водному розчині реагують між собою аргентум(І) нітрат і калій хлорид, одним із продуктів реакції є осад аргентум(І) хлориду:
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Реакції обміну між електролітами у водному розчині.
Завдання скеровано на перевірку вміння застосовувати знання про умови необоротності перебігу реакцій обміну між електролітами в розчині.
Реакції обміну між електролітами в розчинах відбуваються за участю йонів. Умови необоротності перебігу реакцій обміну між електролітами в розчині наведено на схемі (рис. 1).
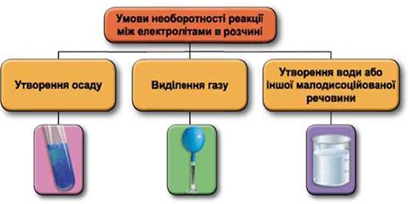
Рис. 1. Умови необоротності реакцій між електролітами у водних розчинах
У водному розчині реагують між собою барій хлорид і сульфатна кислота, одним із продуктів реакції є осад барій сульфату:
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Окисно-відновні реакції.
Завдання скеровано на перевірку вміння визначати ступені окиснення хімічних елементів за формулами речовин і складних йонів, визначати кількість відданих або прийнятих під час окисно-відновних реакцій електронів.
Окисно-відновні реакції супроводжувані переходом або зміщенням валентних електронів від атомів з меншою електронегативністю до атомів з більшою електронегативністю, тобто змінами ступенів окиснення атомів хімічних елементів.
Ступінь окиснення – це умовний цілочисловий заряд на атомі в молекулярній частинці, якого би він набув, якщо відокремити зв’язані з ним електронегативніші атоми разом із парами електронів, що належать зв’язкам. Це ціле число – додатне, від’ємне або нуль.
Алгебрична сума ступенів окиснення всіх атомів у нейтральній молекулі дорівнює нулю, а в йоні – величині його заряду.
Ступені окиснення атомів Гідрогену й Оксигену у складних речовинах зазвичай становлять +1 і –2 відповідно.
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Реакції обміну між електролітами у водному розчині.
Завдання скеровано на перевірку вміння застосовувати знання про умови необоротності перебігу реакцій обміну між електролітами в розчині, складати повні й скорочені йонні та йонно-молекулярні рівняння.
Реакції обміну між електролітами в розчинах відбуваються за участю йонів. Умови необоротності перебігу реакцій обміну між електролітами в розчині наведено на схемі (рис. 1).
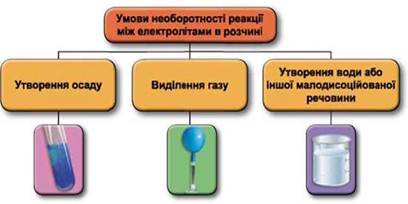
Рис. 1. Умови необоротності реакцій між електролітами у водних розчинах
Взаємодію у водному розчині ферум(ІІ) гідроксиду й хлоридної кислоти описують такими рівняннями:
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Основні класи неорганічних сполук. Луги.
Завдання скеровано на перевірку вміння застосовувати знання про способи добування лугів.
Із-поміж оксидів, яким відповідають основи, формули яких наведено в умові завдання, до активних належить лише барій оксид. Йому відповідає луг – барій гідроксид. Одним зі способів добування лугів є взаємодія оксидів лужних (І А група) і лужноземельних (ІІ А група, починаючи від кальцію) елементів із водою, зокрема барій оксид реагує з нею з утворенням барій гідроксиду:
Відповідь: A.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Основні класи неорганічних сполук. Луги.
Завдання скеровано на перевірку вміння застосовувати знання про способи добування лугів.
Із-поміж гідроксидів, формули яких наведено в умові завдання, до активних належить лише кальцій гідроксид. Одним зі способів добування лугів є взаємодія лужних і лужноземельних металів із водою, зокрема кальцій реагує з нею з утворенням кальцій гідроксиду:
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Основні класи неорганічних сполук. Кислоти.
Завдання скеровано на перевірку вміння застосовувати знання про хімічний склад кислот.
Кислотами називають електроліти, які у водному розчині дисоціюють з утворенням катіонів Гідрогену й аніонів кислотного залишку.
Відповідь: A.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Основні класи неорганічних сполук. Солі.
Завдання скеровано на перевірку вміння розпізнавати формули кислих солей.
Кислі солі – електроліти, які у водному розчині дисоціюють на катіони металічних елементів, Гідрогену й аніони кислотного залишку.
Кислі солі можна розглядати як продукти неповного заміщення атомів Гідрогену багатоосновних кислот металом.
Умову завдання задовольняє натрій гідрогенкарбонат
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічні речовини і їхні властивості. Амфотерність.
Завдання скеровано на перевірку розуміння суті амфотерності й уміння розпізнавати амфотерні оксиди й гідроксиди.
Амфотерністю називають здатність деяких хімічних сполук залежно від умов виявляти або осно́вні, або кислотні властивості. Оксиди й гідроксиди Цинку й Алюмінію виявляють амфотерні властивості:
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічні речовини. Залізо.
Завдання скеровано на перевірку знання хімічних властивостей заліза.
Продуктом реакції заліза з хлором є ферум(ІІІ) хлорид (А).
Продуктом реакції заліза з хлоридною кислотою є ферум(ІІ) хлорид (Б).
Залізо як менш активний метал не може витіснити активніші метали натрій і кальцій із їхніх солей у водних розчинах.
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Періодична система хімічних елементів. Металічні елементи.
Завдання скеровано на перевірку знання структури періодичної системи хімічних елементів.
В атомах металічних елементів на зовнішньому енергетичному рівні перебуває від одного до чотирьох електронів. Кількість електронів в атомах елементів головних підгруп періодичної системи дорівнює номеру групи. Тому варіанти відповіді В й Г не задовольняють умову завдання.
У IV групі містяться неметалічні елементи Карбон і Силіцій.
Із-поміж груп хімічних елементів, про які йдеться в завданні, лише металічні елементи містяться в ІІ групі.
Відповідь: A.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічні речовини. Карбонатна кислота та її солі.
Завдання скеровано на перевірку знання хімічних властивостей карбонатів як солей слабкої та нестійкої карбонатної кислоти.
Солі карбонатної кислоти реагують із кислотами. Характерною ознакою перебігу таких реакцій є виділення вуглекислого газу. Столовий оцет – водний розчин етанової кислоти. Тож між нею і карбонатами Магнію і Кальцію відбуваються такі реакції:
Відповідь: A.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічні речовини. Хімічні властивості алюмінію.
Завдання скеровано на перевірку вміння прогнозувати продукти реакцій за участі алюмінію.
Алюміній сульфат є продуктом реакції між алюмінієм і розведеною сульфатною кислотою:
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічні речовини. Хімічні властивості ферум(ІІІ) гідроксиду.
Завдання скеровано на перевірку вміння прогнозувати продукти реакцій за участі сполук Феруму(ІІІ).
Ферум(ІІІ) гідроксид – нерозчинна основа, унаслідок його термічного розкладання утворюються ферум(ІІІ) оксид і вода:
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічні речовини. Періодична система хімічних елементів. Будова атома. Галогени.
Завдання скеровано на перевірку вміння характеризувати будову атомів хімічних елементів за їхнім місцем у періодичній системі.
Хлор і Йод – елементи VІІ А групи періодичної системи хімічних елементів. Тому спільним у будові їхніх атомів є однакова кількість електронів на зовнішньому енергетичному рівні, яка збігається з номером групи:
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічні речовини. Сульфатна кислота.
Завдання скеровано на перевірку вміння визначати реагенти й продукти в реакціях за участі сульфатної кислоти.
Сульфур(IV) оксид є одним із продуктів реакції між міддю і концентрованою сульфатною кислотою:
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічні речовини. Амоніак.
Завдання скеровано на перевірку знання хімічних властивостей амоніаку.
Амоніак виявляє осно́вні властивості через наявність в атома Нітрогену неподіленої електронної пари. Під час взаємодії з кислотами утворює амонієві солі:
Залежно від мольного відношення продуктом реакції може бути кисла сіль амоній гідрогенсульфат або середня – амоній сульфат:
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічні речовини. Карбон(IV) оксид.
Завдання скеровано на перевірку знання способів добування карбон(IV) оксиду.
Карбон(IV) оксид добувають дією кислот на карбонати:
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Органічні речовини. Гомологічний ряд. Вуглеводні. Алкіни.
Завдання скеровано на перевірку вміння розпізнавати вуглеводні різних гомологічних рядів.
Загальною формулою
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Органічні речовини. Номенклатура алканів.
Завдання скеровано на перевірку вміння називати алкани за систематичною номенклатурою.
Сполуці певної будови відповідає лише одна систематична назва, за якою можна уявити й відтворити будову сполуки, тобто її структурну формулу. Алгоритм побудови назв алканів за систематичною номенклатурою наведено на схемі (рис. 1). Назви алкільних замісників утворюють заміною суфікса -ан у назві алкану на суфікс -ил (-іл). Кількість однакових алкільних замісників позначають множинними префіксами. Два однакові замісники позначають префіксом ди-, три – префіксом три-, чотири – тетра-, п’ять – пента- тощо. Перед приголосними потрібно писати ди-, перед голосними – ді: диметил, але діетил.

Рис. 1. Алгоритм побудови назв алканів за систематичною номенклатурою
В алкані, структурну формулу якого наведено в завданні, вісім атомів Карбону в головному ланцюгу, до третього, четвертого й шостого приєднані вуглеводневі замісники (рис. 2).
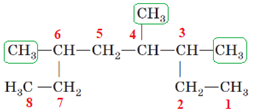
Рис. 2. Структурна формула 3,4,6-триметилоктану
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Органічні речовини. Гомологічні ряди вуглеводнів.
Завдання скеровано на перевірку вміння визначати формули вуглеводнів гомологічного ряду метану.
Загальна формула вуглеводнів гомологічного ряду метану
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Органічні речовини. Ізомерія.
Завдання скеровано на перевірку вміння складати структурні формули ізомерів за молекулярною формулою речовини.
Ізомери – речовини, які мають однаковий якісний і кількісний склад, але різну будову молекул, а тому й різні властивості. Зображення моделей молекул ізомерів складу
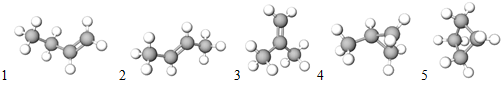
Рис. 1. Ізомери складу
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Органічні речовини. Генетичні зв’язки між класами органічних сполук.
Завдання скеровано на перевірку вміння прогнозувати реагенти й продукти реакцій за участі органічних речовин.
Схемі реакцій, наведеній у завданні, відповідають такі перетворення:
Відповідь: A.
Знайшли помилку? Пишіть на
ТЕМА: Органічні речовини. Ароматичні вуглеводні. Бензен.
Завдання скеровано на перевірку вміння аналізувати рівняння реакцій за участі бензену.
Рівняння реакції бензену з воднем, продуктом якої є циклогексан:
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Органічні речовини. Природні джерела вуглеводнів. Перегонка нафти.
Завдання скеровано на перевірку знання продуктів перегонки нафти.
Нафта – суміш вуглеводнів. Газойль – фракція нафти, суміші вуглеводнів різної будови, переважно
Відповідь: A.
Знайшли помилку? Пишіть на
ТЕМА: Органічні речовини. Фенол.
Завдання скеровано на перевірку знання хімічних властивостей фенолу.
Фенол виявляє слабкі кислотні властивості й реагує з натрій гідроксидом:
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Органічні речовини. Альдегіди.
Завдання скеровано на перевірку знання хімічних властивостей альдегідів.
Речовина
Відповідь: A.
Знайшли помилку? Пишіть на
ТЕМА: Органічні речовини. Естери. Жири.
Завдання скеровано на перевірку знання хімічних властивостей жирів.
Олії – рідкі ненасичені жири, гідруванням їх перетворюють на тверді насичені жири. Тобто правильним є лише друге твердження, бо внаслідок гідролізу жирів утворюються гліцерол і вищі карбонові кислоти.
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Органічні речовини. Вуглеводи.
Завдання скеровано на перевірку вміння розпізнавати моносахариди.
Моносахаридами – простими вуглеводами, що не здатні до гідролізу, є фруктоза й глюкоза.
Відповідь: В.
Знайшли помилку? Пишіть на
ТЕМА: Органічні речовини. Амінокислоти.
Завдання скеровано на перевірку знання складу й властивостей аміноетанової кислоти.
Аміноетанову кислоту (гліцин), як й інші амінокислоти, можна добути гідролізом білка (2). У молекулі аміноетанової кислоти дві характеристичні групи – аміно- й карбоксильна, тому вона є амфотерною сполукою (4).
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Органічні речовини. Високомолекулярні органічні сполуки. Поліетилен.
Завдання скеровано на перевірку розуміння суті термопластичності полімерів, уміння аналізувати спостереження в хімічному експерименті й робити з них висновки.
Термопластичний полімер здатний неодноразово за нагрівання ставати м’якшим, а за охолодження знов тверднути.
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Органічні речовини. Генетичні зв’язки між органічними й неорганічними речовинами.
Завдання скеровано на перевірку вміння встановлювати генетичні зв’язки між органічними й неорганічними речовинами.Органічним продуктом термічного розкладання натрій етаноату є метан:
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Типи хімічних реакцій.
Завдання скеровано на перевірку вміння розпізнавати хімічні реакції різних типів.
У реакцію (1) вступають дві складні речовини, унаслідок реакції утворюється одна складна речовина. Це реакція сполучення (Д).
У реакцію (2) вступають дві складні речовини, унаслідок реакції утворюється дві складні речовини. Це реакція обміну (A).
У реакцію (3) вступає одна складна речовина, унаслідок реакції утворюється одна складна й одна проста речовини. Це реакція розкладання (Г).
У реакцію (4) вступають одна проста й одна складна речовини, унаслідок реакції утворюються одна проста й одна складна речовини. Це реакція заміщення (Б).
Відповідь: 1Д, 2А, 3Г, 4Б.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Типи хімічних реакцій.
Завдання скеровано на перевірку вміння розпізнавати типи хімічних реакцій.
У реакції (1) з низькомолекулярної речовини, молекула якої містить дві характеристичні групи, утворюється високомолекулярна за рахунок реакцій між цими групами сусідніх молекул. Це реакція поліконденсації (В).
У реакції (2) з етанової кислоти й етанолу утворюється етил етаноат – естер. Це реакція естерифікації (Г).
У реакції (3) до молекули етену приєднується молекула води. Це реакція гідратації (А).
У реакції (4) з низькомолекулярної речовини етену, молекула якої містить подвійний зв’язок, утворюється високомолекулярна – поліетилен. Це реакція полімеризації (Б).
Відповідь: 1В, 2Г, 3А, 4Б.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічна хімія. Основні класи неорганічних сполук. Солі.
Завдання скеровано на перевірку знання тривіальних назв солей.
Гіпс (1) –
Алебастр (2) –
Негашене вапно (3) –
Кальцинована сода (4) –
Відповідь: 1В, 2А, 3Д, 4Г.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічна хімія. Основні класи неорганічних сполук.
Завдання скеровано на перевірку вміння розпізнавати неорганічні сполуки різних класів.
Речовина (1) утворена атомами Гідрогену, здатними заміщуватися атомами металічних елементів, і кислотним залишком сульфітної кислоти – сульфітна кислота (Б).
Речовина (2) утворена катіонами Магнію й ортофосфат-аніонами – сіль магній ортофосфат (Д).
Речовина (3) утворена катіонами Кальцію й гідроксид-аніонами – розчинна основа кальцій гідроксид (Г).
Речовина (4) утворена катіонами Кальцію й аніонами Оксигену – основний кальцій оксид (В).
Відповідь: 1Б, 2Д, 3Г, 4В.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Основні класи органічних сполук.
Завдання скеровано на перевірку вміння розпізнавати органічні сполуки різних класів.
Етин (1) – ненасичений вуглеводень, алкін (Г).
Анілін (2) – ароматичний амін, містить характеристичну аміногрупу
Метанол (3) – насичений одноатомний спирт, містить характеристичну гідроксильну групу
Метаналь (4) – альдегід, містить характеристичну альдегідну групу
Відповідь: 1Г, 2Д, 3Б, 4А.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Основні класи органічних сполук.
Завдання скеровано на перевірку знання способів добування органічних речовин.
Анілін (1) добувають відновленням нітробензену (Д):
Фенол (2) добувають гідролізом хлоробензену (А):
Глюкозу (3) добувають гідролізом крохмалю (Г):
Етаналь (4) добувають гідратацією ацетилену (Б):
Відповідь: 1Д, 2А, 3Г, 4Б.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічна хімія. Залізо. Сполуки Феруму.
Завдання скеровано на перевірку вміння визначати склад реагентів і продуктів реакцій за участі заліза й сполук Феруму.
1 Під дією бромідної кислоти (В) залізо перетворюється на ферум(ІІ) бромід:
2 Під дією лугу (Г) у водному розчині ферум(ІІ) бромід перетворюється на ферум(ІІ) гідроксид:
3 Під дією кисню і води (Б) ферум(ІІ) гідроксид перетворюється на ферум(ІІІ) гідроксид:
4 За нагрівання (А) ферум(ІІІ) гідроксид розкладається на ферум(ІІІ) оксид і воду:
Відповідь: 1В, 2Г, 3Б, 4А.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Генетичні зв’язки між класами органічних сполук.
Завдання скеровано на перевірку вміння встановлювати генетичні зв’язки між органічними сполуками різних класів.
Ланцюжок перетворень добування метанової кислоти з речовин, назви яких наведено в умові, такий:
метан (Б) → хлорометан (В) → метанол (Г) → метаналь (А) → метанова кислота.
Рівняння реакцій:
1
2
3
4
Відповідь: 1Б, 2В, 3Г, 4А.
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії. Обчислення за хімічними формулами. Відносна молекулярна маса.
Завдання скеровано на перевірку вміння обчислювати відносну молекулярну масу речовини за її хімічною формулою.
Дано:
Знайти:
Відповідь: 59.
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії. Обчислення за хімічними формулами. Відносна густина газів.
Завдання скеровано на перевірку вміння обчислювати відносну молекулярну масу речовини за її відносною густиною.
Дано:
Знайти:
Відповідь: 64.
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії. Обчислення за хімічними формулами. Кристалогідрати.
Завдання скеровано на перевірку вміння визначати хімічний склад кристалогідрату.
Дано:
Знайти:
Відповідь: 7.
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії. Обчислення за хімічними формулами. Молярний об’єм газів.
Завдання скеровано на перевірку вміння обчислювати об’єм газу за його масою.
Дано:
Знайти:
Відповідь: 56.
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії. Обчислення за хімічними формулами.
Завдання скеровано на перевірку вміння прогнозувати склад молекул за відомою кількістю нуклідів, із яких вони утворені.
Відповідь: 6.
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії. Обчислення за хімічними формулами.
Завдання скеровано на перевірку вміння обчислювати масу хімічного елемента в речовині за її кількістю.
Дано:
Знайти:
Відповідь: 31.
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії. Комбіновані задачі.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 70.
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії. Розчини. Масова частка розчиненої речовини.
Завдання скеровано на перевірку вміння обчислювати масу складника розчину за його масовою часткою.
Дано:
Знайти:
Відповідь: 81.
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії. Комбіновані задачі.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 23.
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії. Комбіновані задачі.
Завдання скеровано на перевірку вміння розв’язувати комбіновані задачі.
Дано:
Знайти:
Відповідь: 81.
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії.
Завдання скеровано на перевірку вміння перетворювати схеми окисно-відновних реакцій на хімічні рівняння методом електронного балансу.
Коефіцієнт перед формулою окисника –
Відповідь: 2.
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії. Виведення молекулярної формули речовини за масовими частками елементів у ній і відносною густиною її пари.
Завдання скеровано на перевірку вміння виводити молекулярну формулу речовини за масовими частками елементів у ній і відносною густиною її пари.
Дано:
Знайти:
Відповідь: 19.
Знайшли помилку? Пишіть на




