ЗНО онлайн 2007 року з хімії – основна сесія
Тестові завдання основної сесії ЗНО 2007 року з хімії
ТЕМА: Загальна хімія. Основні поняття і закони хімії. Закон об’ємних відношень газів.
Завдання скеровано на перевірку розуміння суті закону об’ємних відношень газів.
За однакових умов об’єми газуватих речовин у хімічних реакціях відносяться між собою як невеликі цілі числа – коефіцієнти в рівняннях хімічних реакцій.
Відповідь: A.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Розчини. Масова частка розчиненої речовини.
Завдання скеровано на перевірку розуміння поняття масової частки розчиненої речовини й розчинника.
Масова частка розчиненої речовини – це відношення маси розчиненої речовини до маси розчину. У завданні ідеться про розчин із масовою часткою йоду
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Розчини. Масова частка розчиненої речовини.
Завдання скеровано на перевірку розуміння поняття масової частки розчиненої речовини й розчинника.
Масова частка розчиненої речовини – це відношення маси розчиненої речовини до маси розчину:
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічні речовини та їхні властивості. Оксиди. Несолетворні оксиди.
Завдання скеровано на перевірку вміння розпізнавати несолетворні оксиди.
Класифікацію оксидів за їхнім складом і хімічними властивостями наведено на рисунку 1.
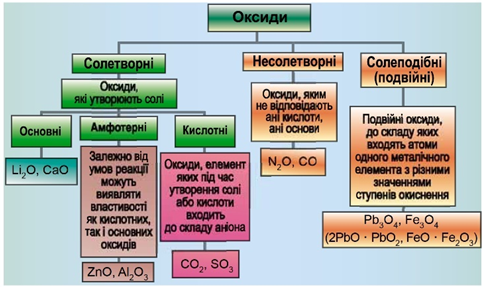
Рис. 1. Класифікація оксидів
Умову завдання задовольняє нітроген(IІ) оксид, який не утворює солей.
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічні речовини та їхні властивості. Кальцій у природі. Сполуки Кальцію.
Завдання скеровано на перевірку знання тривіальних назв деяких сполук Кальцію.
Вапняк і мармур – найважливіші сполуки Кальцію. Їхній головний складник – кальцій карбонат
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічні речовини та їхні властивості. Алюміній у природі. Сполуки Алюмінію.
Завдання скеровано на перевірку знання тривіальних назв деяких сполук Алюмінію.
Головним складником корунду є алюміній оксид
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічна хімія. Неорганічні речовини і їхні властивості. Поняття про твердість (жорсткість) води та способи її усунення.
Завдання скеровано на перевірку знання чинників, що зумовлюють твердість води.
Твердість води – це сукупність її властивостей, зумовлених деякими катіонами металічних елементів у ній. Усі двовалентні катіони тією чи тією мірою впливають на твердість води, оскільки вони взаємодіють із певними аніонами, унаслідок чого утворюються нерозчинні або малорозчинні сполуки, що випадають в осад.
Твердість води переважно зумовлена катіонами
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Вуглеводні. Алкани.
Завдання скеровано на перевірку вміння розпізнавати й складати молекулярні формули алканів.
Суфікс -ан у назві вказує на належність пентану до алканів. Їхня загальна формула –
Умову завдання задовольняє формула
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Оксигеновмісні органічні сполуки. Естери.
Завдання скеровано на перевірку вміння розпізнавати загальну структурну формулу естерів.
Естери – оксигеновмісні органічні сполуки, продукти реакцій між спиртами й карбоновими кислотами.
Загальна структурна формула естерів
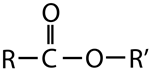
Відповідь: A.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Хімічна формула. Йони.
Завдання скеровано на перевірку вміння аналізувати хімічну формулу речовини.
Хімічна формула – запис, що показує, якісний (визначають за хімічними символами) і кількісний (визначають за правими підрядковими індексами) склад речовини.
Складниками калій гідрогенкарбонату є однозарядні катіони Калію та Гідрогену, двозарядні карбонат-аніон:
Згідно з принципом електронейтральності речовини сума зарядів складників дорівнює нулю.
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Розчини. Електролітична дисоціація.
Завдання скеровано на перевірку вміння аналізувати хімічну формулу речовини й складати рівняння електролітичної дисоціації.
Магній нітрат – сіль, дисоціює у водному розчині на катіони Магнію і нітрат-аніони:
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічна хімія. Металічні елементи. Метали.
Завдання скеровано на перевірку вміння розпізнавати назви металічних елементів.
Лужні елементи належать до першої групи головної підгрупи періодичної системи (рис. 1).
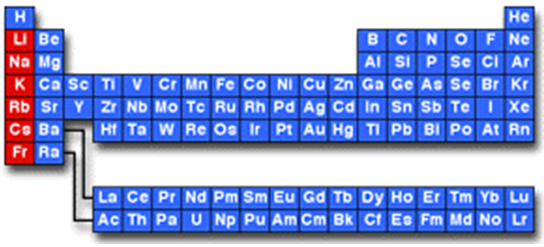
Рис. 1. Місце лужних елементів у періодичній системі
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Основні класи неорганічних сполук. Нерозчинні основи.
Завдання скеровано на перевірку знання складу та властивостей нерозчинних основ.
Нерозчинні основи за нагрівання розкладаються на оксид металічного елемента й воду. Прикладом є термічне розкладання ферум(ІІІ) гідроксиду.
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Періодичний закон і періодична система хімічних елементів. Структура періодичної системи.
Завдання скеровано на перевірку вміння здобувати інформацію з періодичної системи періодичних елементів.
Галогени – елементи VIIА (17) групи періодичної системи. Загальна формула леткої сполуки галогену з Гідрогеном –
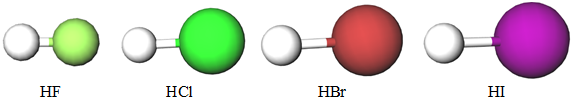
Відповідь: A.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Вуглеводні. Номенклатура алкенів.
Завдання скеровано на перевірку вміння називати алкени за систематичною номенклатурою.
Зі структурної формули, що містить подвійний зв’язок, зрозуміло, що йдеться про назву алкену розгалуженої будови.
Називати алкени за систематичною номенклатурою потрібно за алгоритмом, наведеним на схемі (рис. 1).

Рис. 1. Алгоритм побудови назв алкенів й алкінів за систематичною номенклатурою
Зверніть увагу: положення кратного зв’язку й замісників позначають найменшими числами, але перевагу у виборі початку нумерації віддають кратному зв’язку (рис. 2).
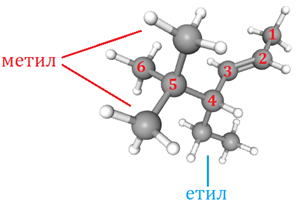
Рис. 2. Модель молекули 4-етил-5,5-диметил-гекс-2-ену
Відповідь: A.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Оксигеновмісні органічні сполуки. Багатоатомні спирти.
Завдання скеровано на перевірку вміння називати багатоатомні спирти за систематичною номенклатурою.
Називати насичені ациклічні спирти за систематичною номенклатурою потрібно за алгоритмом, наведеним на схемі (рис. 1).
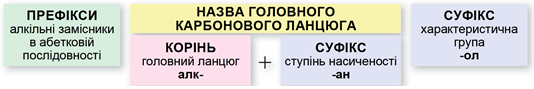
Рис. 1. Алгоритм побудови назв насичених ациклічних спиртів за систематичною номенклатурою
Важливо пам’ятати:
- потрібно нумерувати карбоновий ланцюг із того кінця, до якого ближче розташована гідроксильна група;
- якщо гідроксильна група рівновіддалена від обох кінців головного карбонового ланцюга, то нумерують із того кінця, до якого ближче розташований алкільний замісник;
- якщо гідроксильна група й замісники рівновіддалені від обох кінців головного карбонового ланцюга, то його нумерують так, щоб замісник, назву якого за абеткою вживають раніше, був позначений найменшим числом;
- якщо гідроксильна група й замісники рівновіддалені від обох кінців головного карбонового ланцюга, але з одного кінця замісників більше, то нумерацію проводять з урахуванням положення замісників, позначених найменшими числами.
У молекулі гліцеролу в головному ланцюгу три атоми Карбону, тому корінь у назві – пропан-. Кожен із трьох атомів Карбону сполучений із гідроксильною групою – -триол (рис. 2).
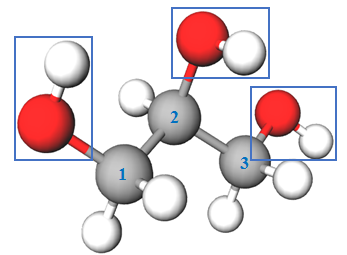
Рис. 2. Модель молекули гліцеролу – 1,2,3-пропантриолу
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Оксигеновмісні органічні сполуки. Вуглеводи.
Завдання скеровано на перевірку вміння розпізнавати формули вуглеводів.
У завданні наведено молекулярну формулу сахарози.
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічна хімія. Металічні елементи. Метали.
Завдання скеровано на перевірку вміння використовувати ряд активності металів для порівняння їхніх властивостей.
Магній у ряду активності розташований лівіше від заліза, тому активніше і, відповідно, швидше реагує з хлоридною кислотою (рис. 1).

Рис. 1. Ряд активності металів
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Будова атома. Валентні електрони.
Завдання скеровано на перевірку вміння аналізувати будову атомів хімічних елементів.
Берилій – четвертий елемент періодичної системи, міститься в другому періоді у IIA групі. В атомі Берилію два енергетичні рівні з чотирма електронами.
Електронна формула атома Берилію в основному стані така:
Тобто в атомі Берилію в основному стані два валентні електрони, орбіталі яких сферичні.
Відповідь: A.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Будова атома. Валентні електрони.
Завдання скеровано на перевірку розуміння особливостей утворення ковалентного зв’язку за донорно-акцепторним механізмом.
Ковалентний зв’язок може утворюватися за обмінним (унаслідок усуспільнення електронів) або за донорно-акцепторним механізмом.
За донорно-акцепторним механізмом один атом надає електронну пару в спільне користування. Катіон амонію, наприклад, утворюється внаслідок приєднання протона
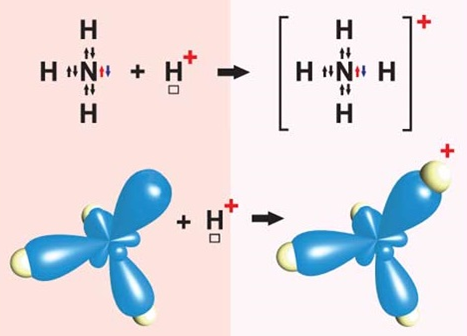
Рис. 1. Утворення катіона амонію
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Основні класи неорганічних сполук. Кислотні оксиди.
Завдання скеровано на перевірку вміння прогнозувати продукти реакцій між неорганічними сполуками – представниками різних класів.
Сульфур(VI) оксид – кислотний, йому відповідає двоосновна сульфатна кислота. Тож сульфур(VI) оксид реагує з калій гідроксидом у водному розчині з утворенням калій сульфату й води:
Утворення калій гідрогенсульфату – кислої солі – неможливе, бо в калій гідроксид узято в надлишку.
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічна хімія. Металічні елементи. Метали. Сульфатна кислота. Властивості концентрованої сульфатної кислоти.
Завдання скеровано на перевірку вміння прогнозувати можливість реакції між металом і концентрованою сульфатною кислотою.
Концентрована сульфатна кислота реагує з багатьма металами, продукти реакцій наведено на схемі (рис. 1).
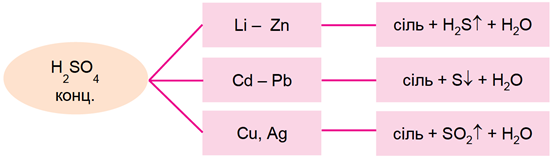
Рис. 1. Продукти реакцій металів із концентрованою сульфатною кислотою
Із-поміж металів, хімічні формули яких наведено у варіантах відповіді, лише золото стійке до дії концентрованої сульфатної кислоти.
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічна хімія. Металічні елементи. Метали. Витискувальний ряд металів.
Завдання скеровано на перевірку вміння аналізувати реакції металів із солями.
Цинк – активніший за мідь метал, бо розташований лівіше від неї в ряду активності (рис. 1).

Рис. 1. Ряд активності металів
Тому цинк відновлює мідь із розчину солі Купруму(ІІ):
Відповідь: A.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Кислоти. Електролітична дисоціація кислот.
Завдання скеровано на перевірку розуміння електролітичної дисоціації кислот.
Універсальний індикаторний папір змінює забарвлення на червоне в кислому середовищі. Тобто в досліджуваному розчині є катіони Гідрогену.
Відповідь: A.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічна хімія. Оксиген. Озон.
Завдання скеровано на перевірку знання властивостей озону.
Озон – газ блакитного кольору, дуже активний, розчинний у воді, його молекула має кутову будову.
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Оксигеновмісні органічні сполуки. Ароматичні вуглеводні. Бензен.
Завдання скеровано на перевірку знання будови молекули бензену.
Молекула бензену має циклічну будову, атоми Карбону сполучені між собою особливими хімічними зв’язками, проміжними за довжиною і деякими іншими характеристиками між подвійним (ненасиченим) і простим (насиченим).
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Нітрогеновмісні органічні сполуки. Анілін – ароматичний амін.
Завдання скеровано на перевірку розуміння взаємного впливу груп атомів у молекулі аніліну.
Неподілена електронна пара атома Нітрогену взаємодіє з ароматичною системою зв’язків і частково зміщується від атома Нітрогену до бензенового кільця. Унаслідок цього на атомі Нітрогену електронна густина зменшується, і тому зменшуються основні властивості аміногрупи (рис. 1), а кислотні властивості посилюються. Адже протон притягається слабше й відщеплюється легше.
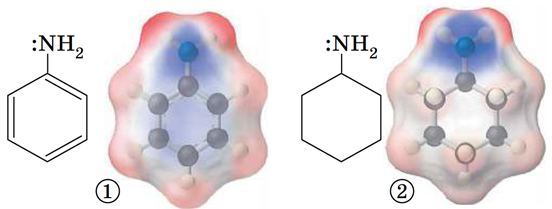
Рис. 1. Розподіл електронної густини в молекулах аніліну (1) і циклогексан-1-аміну (2)
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Суміші. Відносна густина газу.
Завдання скеровано на перевірку вміння аналізувати склад газової суміші й застосовувати закон об’ємних відношень газів.
Дано:
Знайти:
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Суміші. Розчини. Розчинність речовин.
Завдання скеровано на перевірку вміння порівнювати розчинність речовин.
Целюлоза – біополімер, у воді не розчиняється.
Ацетилен – малорозчинний у воді газ.
Кальцій сульфат – малорозчинна речовина, а барій гідроксид – луг, який добре розчиняється у воді. Про це можна дізнатися з таблиці «Розчинність кислот, основ, амфотерних гідроксидів і солей у воді за температури 20–25 °С».
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічна хімія. Металічні елементи. Метали. Способи добування металів.
Завдання скеровано на перевірку розуміння хімізму пірометалургійних процесів.
Пірометалургія об’єднує хімічні способи відновлення металів із руд за високої температури.
Як відновники в пірометалургії використовують вугілля (кокс), карбон(ІІ) оксид, водень, активні метали, силіцій.
Наприклад, для добування металів пірометалургійним способом із сульфідних руд їх спочатку випалюють:
Відповідь: A.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічна хімія. Неметалічні елементи. Карбон. Алмаз.
Завдання скеровано на перевірку розуміння зумовленості застосування речовин їхніми властивостями.
Алмаз вирізняється високою твердістю, тому його використовують у виробництві шліфувальних матеріалів.
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Оксигеновмісні органічні сполуки. Фенол.
Завдання скеровано на перевірку знання способів добування та впливу на довкілля фенолу.
Фенол видобувають із кам’яновугільної смоли. Фенол — токсична речовина, забруднювач довкілля.
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Нітрогеновмісні органічні сполуки. Амінокислоти. Білки.
Завдання скеровано на перевірку розуміння значення біотехнологічних процесів.
Біотехнологія – це наука про технології створення і використання біологічних об’єктів, що сприяють інтенсифікації виробництва або створенню нових видів продуктів різного призначення на основі методів клітинної та генетичної інженерії. Біотехнологічне виробництво є складним комплексом біофізичних, біохімічних і фізико-хімічних процесів, у яких тісно взаємопов’язані виробництво та біологія.
Наслідком біотехнологічних процесів розмноження деяких мікроорганізмів є нарощування значної біомаси протягом короткого часу. У промислових масштабах вже протягом багатьох десятиліть використовують здатність мікроорганізмів перетворювати рослинну біомасу з низьким вмістом білка на харчові продукти з високим його вмістом.
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Нітрогеновмісні органічні сполуки. Амінокислоти. Білки. Нуклеїнові кислоти.
Завдання скеровано на перевірку розуміння ролі нуклеїнових кислот у передаванні генетичної інформації.
Передавання інформації відбувається завдяки здатності ДНК до реплікації (від лат. replicatio – відбиття). ДНК подвоюється, щоби забезпечити дочірню клітину повним набором відповідних молекул. У момент поділу клітини розриваються водневі зв’язки, подвійна спіраль починає розкручуватися, розділяючись на два ланцюги. На кожному з них добудовується додатковий ланцюг за рахунок нуклеотидів, що надходять із навколишнього середовища й розміщуються за принципом комплементарності. Між азотистими основами утворюються нові водневі зв’язки. У результаті відбувається точне відтворення початкової подвійної спіралі.
Відповідь: A.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічна хімія. Неметалічні елементи. Азот. Амоніак.
Завдання скеровано на перевірку вміння виявляти гідроксид-аніони в розчині.
Нашатирний спирт – тривіальна назва водного розчину амоніаку. Середовище водного розчину амоніаку лужне, бо містить гідроксид-аніони, що утворюються внаслідок взаємодії молекул амоніаку з молекулами води:
Відповідь: Б.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Ароматичні вуглеводні. Бензен.
Завдання скеровано на перевірку знання хімічних властивостей бензену.
За надлишку хлору можна замістити на атоми Хлору всі атоми Гідрогену бензенового циклу:
Відповідь: B.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Оксигеновмісні органічні сполуки. Багатоатомні спирти.
Завдання скеровано на перевірку знання якісної реакції на багатоатомні спирти.
Якісна реакція на гліцерол пов’язана з тим, що в його молекулі є три гідроксильні групи
Відповідь: A.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Оксигеновмісні органічні сполуки. Багатоатомні спирти.
Завдання скеровано на перевірку знання якісної реакції на багатоатомні спирти.
Якісна реакція на гліцерол пов’язана з тим, що в його молекулі є три гідроксильні групи
Для добування купрум(ІІ) гідроксиду потрібно використати мідний купорос і натрій гідроксид.
Відповідь: Г.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Основні класи неорганічних сполук.
Завдання скеровано на перевірку вміння прогнозувати продукти реакцій між неорганічними сполуками різних класів.
Унаслідок реакції нейтралізації барій гідроксиду нітратною кислотою утворюються барій нітрат і вода:
Унаслідок реакції між барій хлоридом і калій сульфатом у водному розчині утворюються калій хлорид і нерозчинний барій сульфат:
Унаслідок дії сильної нелеткої сульфатної кислоти на натрій хлорид – сіль леткої хлоридної кислоти – утворюється натрій гідрогенсульфат і виділяється газуватий гідроген хлорид:
Відповідь: 2В, 3А, 4Б.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Основні класи неорганічних сполук. Якісні реакції на деякі йони.
Завдання скеровано на перевірку вміння прогнозувати продукти реакцій за участі деяких йонів.
Скорочені йонні рівняння реакцій, про які йдеться в завданні, такі:
Відповідь: 1Г, 2А, 3Б, 4В.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Основні класи неорганічних сполук. Луги й нерозчинні основи.
Завдання скеровано на перевірку знання хімічних властивостей лугів і нерозчинних основ.
Нерозчинні основи за нагрівання розкладаються на відповідний оксид і воду.
Луги реагують із солями у водних розчинах, якщо хоча б один з продуктів реакції обміну між ними – основа чи сіль – є нерозчинним.
Відповідь: 3Б, 4А.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Ненасичені вуглеводні. Типи гібридизації атомів Карбону в молекулах етену й етину.
Завдання скеровано на перевірку знання електронної будови молекул етену й етину.
У молекулі етену атоми Карбону перебувають у стані
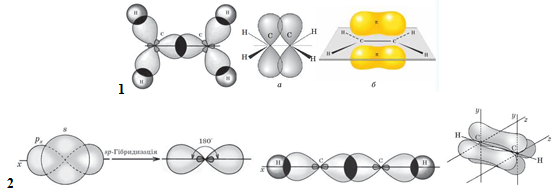
Рис. 1. Гібридизація електронних хмар атомів Карбону в молекулах етену (1) й етину (2)
Відповідь: 2Б, 3А.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Хімічний зв’язок. Будова речовини.
Завдання скеровано на перевірку розуміння зумовленості властивостей речовини її будовою.
Усі метали є провідниками електричного струму.
Розплави електролітів проводять електричний струм.
Поміж речовин із ковалентним неполярним типом зв’язку є як діелектрики, так і напівпровідники.
У речовин із ковалентним полярним типом зв’язку порівняно невисокі температури плавлення.
Відповідь: 1Б, 2Г, 3В, 4А.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Хімічний зв’язок. Будова речовини.
Завдання скеровано на перевірку розуміння зумовленості властивостей речовини її будовою.
Металічний зв’язок за рахунок усуспільнених електронів – електронного газу – між атомами та катіонами Купруму в кристалі міді.
Йонний зв’язок між катіонами Кальцію і флуорид-аніонами в кристалі кальцій флуориду.
Ковалентний полярний зв’язок між атомами Гідрогену й Хлору в молекулі гідроген хлориду.
Ковалентний неполярний зв’язок між атомами Нітрогену в молекулі азоту.
Відповідь: 1Г, 2А, 3Б, 4В.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Періодичний закон і періодична система хімічних елементів. Будова атома. Електронегативність.
Завдання скеровано на перевірку розуміння закономірностей зміни електронегативності в періодичній системі хімічних елементів.
У періоді зі збільшенням протонного числа хімічних елементів збільшується електронегативність. Усі хімічні елементи, символи яких наведено в умові, належать до третього періоду, тобто їхня електронегативність зростає в такій послідовності:
Відповідь: Г А В Б.
Знайшли помилку? Пишіть на
ТЕМА: Загальна хімія. Розчини. Електролітична дисоціація. Сила кислот.
Завдання скеровано на перевірку розуміння закономірностей зміни сили кислот – водних розчинів гідроген галогенідів.
У підгрупі галогенів зі збільшенням протонного числа хімічних елементів збільшується ступінь дисоціації і, відповідно, сила кислот. Це зумовлено зменшенням електронегативності і збільшенням радіуса атомів галогенів, збільшенням довжини зв’язку
Відповідь: В А Г Б.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічна хімія. Неметалічні елементи. Сполуки Нітрогену.
Завдання скеровано на перевірку вміння встановлювати генетичні зв’язки між сполуками Нітрогену.
Генетичний ланцюжок добування нітратної кислоти такий:
Відповідь: Г В А Б.
Знайшли помилку? Пишіть на
ТЕМА: Неорганічна хімія. Неметалічні елементи. Сполуки Cульфуру. Виробництво сульфатної кислоти.
Завдання скеровано на перевірку вміння встановлювати генетичні зв’язки між сполуками Сульфуру, знання хімізму виробництва сульфатної кислоти.
Генетичний ланцюжок виробництва сульфатної кислоти із сірки такий:
Відповідь: В А Б Г.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Вуглеводні. Генетичні зв’язки між вуглеводнями.
Завдання скеровано на перевірку вміння встановлювати генетичні зв’язки між вуглеводнями різних груп.
Генетичний ланцюжок добування циклогексану такий:
Відповідь: В Б А Г.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Основні класи органічних сполук. Генетичні зв’язки між органічними сполуками різних класів.
Завдання скеровано на перевірку вміння встановлювати генетичні зв’язки між органічними сполуками різних класів.
Генетичний ланцюжок добування метанамоній хлориду такий:
Відповідь: Г Б А В.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Основні класи органічних сполук. Генетичні зв’язки між органічними сполуками різних класів.
Завдання скеровано на перевірку вміння встановлювати генетичні зв’язки між органічними сполуками різних класів.
Генетичний ланцюжок синтезу дипептиду такий:
Відповідь: В Г А Б.
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії. Окисно-відновні реакції.
Завдання скеровано на перевірку вміння перетворювати схеми окисно-відновних реакцій на хімічні рівняння методом електронного балансу.
Сума коефіцієнтів перед формулами реагентів –
Відповідь: 14.
Знайшли помилку? Пишіть на
ТЕМА: Основні поняття і закони хімії. Закон збереження маси речовин. хімічні рівняння.
Завдання скеровано на перевірку вміння застосовувати закон збереження маси речовини для записування хімічних рівнянь.
Сума коефіцієнтів у хімічному рівнянні –
Відповідь: 12.
Знайшли помилку? Пишіть на
ТЕМА: Органічна хімія. Вуглеводні. Метан. Хлорування метану.
Завдання скеровано на перевірку знання хімічних властивостей метану.
У завданні йдеться про продукти реакції заміщення за участі метану й хлору:
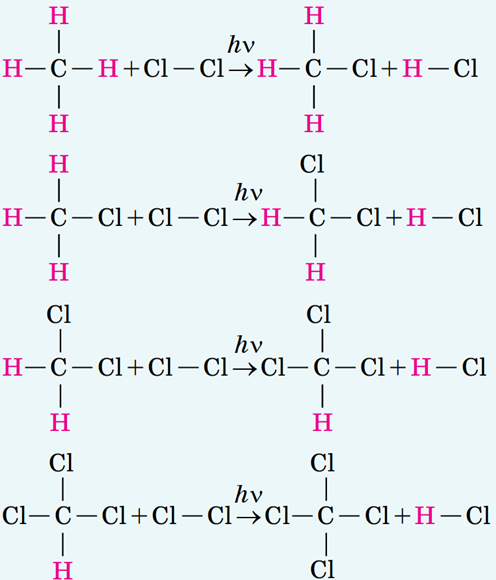
Відповідь: 4.
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії. Окисно-відновні реакції.
Завдання скеровано на перевірку вміння перетворювати схеми окисно-відновних реакцій на хімічні рівняння методом електронного балансу.
Загальна кількість прийнятих електронів в електронному балансі –
Відповідь: 4.
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії. Класифікація хімічних реакцій. Екзо- й ендотермічні реакції. Окисно-відновні реакції.
Завдання скеровано на перевірку вмінь класифікувати хімічні реакції та перетворювати схеми окисно-відновних реакцій на хімічні рівняння методом електронного балансу.
До екзотермічних реакцій із-поміж тих, фрагменти схем яких наведено в умові, належить повне окиснення фосфіну:
Загальна кількість прийнятих електронів в електронному балансі –
Відповідь: 4.
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії. Суміші. Розчини. Визначення кількісного складу розчину.
Завдання скеровано на перевірку вміння визначати кількісний склад розчину.
Дано:
Знайти:
Відповідь: 100.
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії. Обчислення за хімічним рівнянням маси продукту реакції за відомою масою реагенту, що містить домішки.
Завдання скеровано на перевірку вміння обчислювати за хімічним рівнянням масу продукту реакції за відомою масою реагенту, що містить домішки.
Дано:
Знайти:
Відповідь: 112.
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії. Обчислення за хімічним рівнянням маси продукту реакції за відомим об’ємом реагенту.
Завдання скеровано на перевірку вміння обчислювати за хімічним рівнянням масу продукту реакції за відомим об’ємом реагенту.
Дано:
Знайти:
Відповідь: 900.
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії. Обчислення за хімічним рівнянням. Розв’язування комбінованих задач.
Завдання скеровано на перевірку вміння розв’язувати за хімічними рівняннями комбіновані задачі.
Дано:
Знайти:
Відповідь: 186.
Знайшли помилку? Пишіть на
ТЕМА: Обчислення в хімії. Визначення хімічної формули речовини за кількісними даними щодо реакції за її участі.
Завдання скеровано на перевірку вміння визначати хімічну формулу речовини за кількісними даними щодо реакції за її участі.
Дано:
Знайти:
Відповідь: ЕТАНОЛ.
Знайшли помилку? Пишіть на




